题目内容
金属钛对人体无毒且有惰性,能与肌肉和骨髓生长在一起,因而有“生物金属”之称。下列有关 和
和 的说法中不正确的是
的说法中不正确的是
 和
和 的说法中不正确的是
的说法中不正确的是A. 和 和 属于同种元素 属于同种元素 | B. 和 和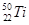 的质量数相同 的质量数相同 |
C. 的相对原子质量约为48 的相对原子质量约为48 | D. 和 和 为不同的核素,互为同位素 为不同的核素,互为同位素 |
B
在表示原子组成时,元素符号的左下角表示的是质子数,左上角表示的是质量数。 和
和 的质子数均是22,但质量数不同,分别是48和50,所以这两种核素互为同位素。由于电子的质量很小,所以质量数近似等于原子的相对原子质量,因此选项B是错误的,所以答案选B。
的质子数均是22,但质量数不同,分别是48和50,所以这两种核素互为同位素。由于电子的质量很小,所以质量数近似等于原子的相对原子质量,因此选项B是错误的,所以答案选B。
 和
和 的质子数均是22,但质量数不同,分别是48和50,所以这两种核素互为同位素。由于电子的质量很小,所以质量数近似等于原子的相对原子质量,因此选项B是错误的,所以答案选B。
的质子数均是22,但质量数不同,分别是48和50,所以这两种核素互为同位素。由于电子的质量很小,所以质量数近似等于原子的相对原子质量,因此选项B是错误的,所以答案选B。
练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目