题目内容
15.把CO2通入含NaOH 0.8g的碱溶液中,将产物在减压条件下蒸干后,得固体1.37g,则通入CO2的质量是( )| A. | 0.44 g | B. | 0.88 g | C. | 0.66 g | D. | 都不是 |
分析 首先根据NaOH的质量和固体的质量判断反应产物的成分,利用假设法进行,假定0.8g氢氧化钠全部生成碳酸钠,0.8g氢氧化钠全部生成碳酸氢钠,计算碳酸钠与碳酸氢钠的质量,根据实际固体质量判断产物成分,再根据钠元素守恒与得到固体质量列方程计算各组分的物质的量,根据碳元素守恒计算二氧化碳的质量.
解答 解:设0.8g氢氧化钠全部生成碳酸钠,质量为x,则有
2NaOH+CO2=Na2CO3+H2O
80 106
0.8g x
x=$\frac{0.8g×106}{80}$=1.06g,
设0.8g氢氧化钠全部生成碳酸氢钠,质量为y,则有
NaOH+CO2=NaHCO3
40 84
0.8g y
y=$\frac{0.8g×84}{40}$=1.68g,
而题干中给出的物质的质量为1.37g,所以产物为碳酸钠、碳酸氢钠.
设混合物中含有mmolNa2CO3,nmolNaHCO3,根据钠元素守恒有:2m+n=$\frac{0.8}{40}$,根据固体质量有:106m+84n=1.37,联立方程解得:m=0.005,n=0.01,所以通入CO2的质量为:(0.005+0.01)mol×44g/mol=0.66g,
故选:C.
点评 本题考查化学方程式的计算,根据反应物的量利用极限法判断生成物的组成为解答该题的关键,题目难度中等.

练习册系列答案
相关题目
5.NA代表阿伏加德罗常数的数值,下列有关NA的叙述中,正确的是( )
| A. | 1mol任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L SO3中所含分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol氯气失去电子的数目为2NA个 |
3.下列说法正确的是( )
| A. | 明矾可用于水的消毒、杀菌 | B. | NaHCO3可用于治疗胃酸过多 | ||
| C. | 浓硝酸保存于无色玻璃瓶中 | D. | 氢氟酸可保存于玻璃瓶中 |
7.某工业废水仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1mol/L (此数值忽略水的电离及离子的水解)
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加.
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰.
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2 溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、NH4+、Cu2+.
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是6I-+2NO3-+8H+═3I2+2NO↑+4H2O.
(3)甲同学最终确定原溶液中所含阳离子有Mg2+、Al3+,阴离子有Cl-、I-、NO3-、SO42-;并据此推测原溶液应该呈酸性,原因是Mg2++2H2O?Mg(OH)2+2H+、Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)另取100mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为Mg2++2OH-═Mg(OH)2↓、Al3++4OH-═AlO2-+2H2O.充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为0.4g.
| 阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 阴离子 | Cl- CO32- NO3 - SO42- I- |
Ⅰ.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加.
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰.
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2 溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、NH4+、Cu2+.
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是6I-+2NO3-+8H+═3I2+2NO↑+4H2O.
(3)甲同学最终确定原溶液中所含阳离子有Mg2+、Al3+,阴离子有Cl-、I-、NO3-、SO42-;并据此推测原溶液应该呈酸性,原因是Mg2++2H2O?Mg(OH)2+2H+、Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)另取100mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为Mg2++2OH-═Mg(OH)2↓、Al3++4OH-═AlO2-+2H2O.充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为0.4g.
12.可燃冰是天然气与水在一定条件下相互作用形成的晶体.据测定每0.1m3固体“可燃冰”能释放20m3的甲烷气体,则下列说法中不正确的是( )
| A. | 可燃冰释放的甲烷属于烃 | B. | 可燃冰是水变油,属于化学变化 | ||
| C. | 甲烷与异丁烷为同系物 | D. | 天然气是一种重要的化工原料 |
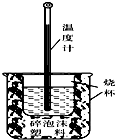 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题: