题目内容
3.与1L 0.1 mol•L-1 的Na2CO3溶液中含有的钠离子个数相等的是( )| A. | 6.02×1022个Na+ | B. | 0.1mol NaCl | ||
| C. | 1L 0.1mol•L-1 Na0H溶液 | D. | 28.6g Na2CO3•10H20 |
分析 1L 0.1 mol•L-1 的Na2CO3溶液中含有的Na2CO3的物质的量n=CV=0.1mol/L×1L=0.1mol,而0.1molNa2CO3中含0.2mol钠离子,个数为0.2NA个.
A、6.02×1022个钠离子为0.1NA个;
B、1mol氯化钠中含1mol钠离子;
C、氢氧化钠的物质的量n=CV=0.1mol/L×1L=0.1mol;
D、求出Na2CO3•10H20的物质的量n=$\frac{28.6g}{286g/mol}$=0.1mol,然后根据1molNa2CO3•10H20中含2mol钠离子来分析.
解答 解:1L 0.1 mol•L-1 的Na2CO3溶液中含有的Na2CO3的物质的量n=CV=0.1mol/L×1L=0.1mol,而0.1molNa2CO3中含0.2mol钠离子,个数为0.2NA个.
A、6.02×1022个钠离子为0.1NA个,不符合题意,故A错误;
B、1mol氯化钠中含1mol钠离子,故0.1mol氯化钠中含0.1mol钠离子即0.1NA个,不符合题意,故B错误;
C、氢氧化钠的物质的量n=CV=0.1mol/L×1L=0.1mol,故含0.1mol钠离子即0.1NA个,不符合题意,故C错误;
D、求出Na2CO3•10H20的物质的量n=$\frac{28.6g}{286g/mol}$=0.1mol,而1molNa2CO3•10H20中含2mol钠离子,故0.1molNa2CO3•10H20中含0.2mol钠离子即0.2NA个,故D正确.
故选D.
点评 本题考查了物质中离子个数的有关计算,熟练掌握公式的运用和物质的结构是解题的关键,难度不大.

练习册系列答案
相关题目
14.在下列酸性溶液中,因发生氧化还原反应而不能大量共存的是( )
| A. | Ag+、NO3-、Cl-、K+ | B. | Cu2+、NH4+、Br-、OH- | ||
| C. | Ag+、Ba2+、OH-、SO42- | D. | Fe2+、Na+、NO3-、SO42- |
15.下列物质间的转化不能通过一步转化实现的是( )
| A. | Na2CO3→Na0H | B. | Fe→Cu | C. | Cu→Cu(OH)2 | D. | CaCl2→CaCO3 |
12.短周期元素W、X、Y、Z原子序数依次增大,其中X是空气中含量最多的元素,Y是地壳含量最多的元素.W和Z原子的最外层电子数相等,且W和Z的核外电子数之和为12,根据以上叙述,下列说法中正确的是( )
| A. | X、Y、Z三种元素的简单离子半径逐渐增大 | |
| B. | W、Y、Z三种元素可形成一种离子化合物,其中各原子均满足8电子稳定结构 | |
| C. | W和Y、Y和Z均能形成原子个数比为1:1的化合物,这两种化合物中均含有极性共价键和非极性共价键 | |
| D. | 相同条件下,Z的最高价氧化物对应的水化物的pH大于W、X、Y三种元素形成的化合物的溶液 |
1.目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位.镍能形成多种不同的化合物.图1是镍的一种配合物的结构,图2是一种镍的氧合物的晶胞.判断下列说法正确的是( )
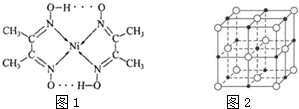

| A. | 图2可能表示的是氧化镍(NiO)的晶胞 | |
| B. | 图1中C、N、O的第一电离能C>N>O | |
| C. | 图2中离镍原子最近的镍原子数共为8个 | |
| D. | 图1分子中存在的化学键有共价键、配位键、氢键 |