题目内容
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g) +B(g)![]() 2C(g),2 s后测得C的浓度为0.6 mol·L-1,下列说法正确的是( )
2C(g),2 s后测得C的浓度为0.6 mol·L-1,下列说法正确的是( )
A. 用物质A表示的反应平均速率为0.6 mol·L-1·s-1
B. 用物质B表示的反应的平均速率为0.3 mol·L-1·s-1
C. 2s时物质A的转化率为30%
D. 2s时物质B的浓度为0.8mol·L-1
【答案】C
【解析】
A.根据方程式知,△c(A)=△c(C)=0.6mol/L,则A的平均反应速率为:![]() =0.3mol/(L·s),故A错误;
=0.3mol/(L·s),故A错误;
B.△c(B)=![]() ×0.6mol/L=0.3mol/L,υ(B)=
×0.6mol/L=0.3mol/L,υ(B)=![]() =0.15mol/(L·s),故B错误;
=0.15mol/(L·s),故B错误;
C.A的起始浓度是2mol/L,根据方程式知,△c(A)=△c(C)=0.6mol/L,故A的转化率=![]() ×100%=30%,故C正确;
×100%=30%,故C正确;
D.B的起始浓度是1mol/L,根据方程式知,△c(B)=![]() ×0.6mol/L=0.3mol/L,2s时物质B的浓度为:1mol/L-0.3mol/L=0.7 mol/L,故D错误;
×0.6mol/L=0.3mol/L,2s时物质B的浓度为:1mol/L-0.3mol/L=0.7 mol/L,故D错误;
故答案为C。

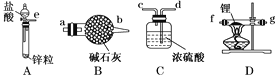
【题目】某小组拟用酸性KMnO4溶液与H2C2O4溶液的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L酸性KMnO4溶液)/mL | m(MnSO4)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.5 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |