题目内容
 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
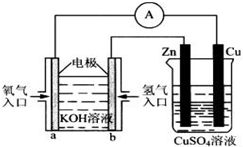
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )分析:左边装置是原电池,氢氧原料原电池中,投放燃料的电极是负极,负极上失电子发生氧化反应,投放氧化剂的电极是正极,正极上发生还原反应;右边装置是电解池,电解池阳极上失电子发生氧化反应,阴极上得电子发生还原反应,据此分析解答.
解答:解:A、右边装置是电解池,铜电极连接原电池的正极,所以铜电极是电解池的阳极,故A正确.
B、根据放电过程中,根据得失电子数相等计算消耗氧气的体积,设消耗氧气的体积为v.
根据得失电子数相等得氧气和铜的关系式为:
O2------2Cu
22.4L 128g
V 12.8g
V=
=2.24L,故B正确.
C、左边装置是原电池,负极上氢气失电子和氢氧根离子反应生成水,电极反应式为:H2+2OH--2e-═2H2O,故C正确.
D、左边装置是原电池,正极上氧气得电子发生还原反应,故D错误.
故选D.
B、根据放电过程中,根据得失电子数相等计算消耗氧气的体积,设消耗氧气的体积为v.
根据得失电子数相等得氧气和铜的关系式为:
O2------2Cu
22.4L 128g
V 12.8g
V=
| 12.8g×22.4L |
| 128g |
C、左边装置是原电池,负极上氢气失电子和氢氧根离子反应生成水,电极反应式为:H2+2OH--2e-═2H2O,故C正确.
D、左边装置是原电池,正极上氧气得电子发生还原反应,故D错误.
故选D.
点评:本题考查了原电池和电解池原理,难度不大,注意氢氧燃料电池中电极反应式的书写,书写时要结合电解质溶液的酸碱性,酸碱性不同,电极反应式的书写不同.

练习册系列答案
相关题目
到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源.请回答下列问题:
(1)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2599kJ?mol-1,则乙炔的燃烧热为 .
(2)有些反应进行得很慢,有些反应不容易直接发生,有些反应的产品不纯(有副反应发生),这给测定反应热造成了困难,此时可利用盖斯定律,就可以间接地把它们的反应热计算出来.已知
①CO(g)+
O2(g)═CO2(g)△H1=-283.0kJ?mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
则C(s)+
O2(g)=CO(g)△H= .
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.已知键能数据如表.
反应N2+3H2?2NH3△H=a kJ?mol-1.试根据表中所列键能数据估算a= .
(1)2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2599kJ?mol-1,则乙炔的燃烧热为
(2)有些反应进行得很慢,有些反应不容易直接发生,有些反应的产品不纯(有副反应发生),这给测定反应热造成了困难,此时可利用盖斯定律,就可以间接地把它们的反应热计算出来.已知
①CO(g)+
| 1 |
| 2 |
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
则C(s)+
| 1 |
| 2 |
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.已知键能数据如表.
| 化学键 | 键能(kJ/mol) | 化学键 | 键能(kJ/mol) |
| N≡N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
 Ⅰ.用碳棒作电极,电解下列水溶液:①Na2SO4溶液 ②AgNO3溶液 ③KCl溶液 ④CuCl2溶液.通过相同电量时,阴极产生的气体物质的量相同的是(填序号)
Ⅰ.用碳棒作电极,电解下列水溶液:①Na2SO4溶液 ②AgNO3溶液 ③KCl溶液 ④CuCl2溶液.通过相同电量时,阴极产生的气体物质的量相同的是(填序号)