题目内容
12.实现Al3++3A1O2-+6H2O═4Al(OH)3↓,正确的做法是( )| A. | 向偏铝酸钠溶液中不断滴入盐酸溶液 | |
| B. | 向烧碱溶液中不断滴入铝盐溶液 | |
| C. | 向碳酸溶液中不断滴入偏铝酸钠溶液 | |
| D. | 向铝盐溶液中不断滴入烧碱溶液 |
分析 Al3++3A1O2-+6H2O═4Al(OH)3↓,表示可溶性铝盐与可溶性偏铝酸盐发生双水解反应生成氢氧化铝沉淀,据此解答.
解答 解:A.向NaAlO2溶液中不断滴入盐酸,发生反应为A1O2-+H2O+H+═Al(OH)3↓,Al(OH)3+3H+═Al3++3H2O,故A错误;
B.向烧碱溶液中不断滴入铝盐溶液,反应开始时碱过量,没有沉淀生成,先生成AlO2-离子,当碱全部反应后,再加入铝盐,发生反应Al3++3AlO2-+6H2O=4Al(OH)3↓,故B正确;
C.向碳酸溶液中不断滴入偏铝酸钠溶液,二氧化碳、水与偏铝酸钠反应生成碳酸氢钠和氢氧化铝,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故C错误;
D.向铝盐溶液中不断加入NaOH溶液,发生反应为Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═A1O2-+2H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确铝离子与偏铝酸根离子的双水解是解题关键,题目难度中等.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
20.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl-、SO42- | |
| B. | 酸性溶液中可能大量存在Na+、ClO-、SO42-、I- | |
| C. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、Cl-、HCO3- |
7.下列离子可能大量共存的是( )
| A. | 无色溶液:Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液:Na+、ClO?、SO42?、I? | |
| C. | 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- | |
| D. | 常温下,水电离出的c(H+)=1×10-13 mol•L-1的溶液:K+、Na+、Cl-、S2- |
17.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列正确的是( )
| A. | 原子半径的大小顺序:Y>Z>W>X | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Z弱 | |
| C. | 化合物YX、ZX2、WX3中化学键类型相同 | |
| D. | 元素W的简单气态氢化物的热稳定性比X强 |
4.下列化学用语正确的是( )
| A. | 乙烯的结构式:CH2=CH2 | B. | Clˉ的结构示意图: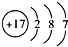 | ||
| C. | I-131:${\;}_{53}^{78}$I | D. | Na2S 的电子式: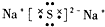 |
2.如图是某学校实验室从化学试剂商店买回的硝酸试剂标签上的部分内容.据此下列说法错误的是( )

| A. | 该硝酸的物质的量浓度约为15.1mol•L-1 | |
| B. | 0.3molCu与足量的该硝酸反应产生6gNO | |
| C. | 该硝酸盛放在棕色的玻璃试剂瓶中 | |
| D. | 等体积的水与该硝酸混合所得溶液的溶质质量分数大于34% |
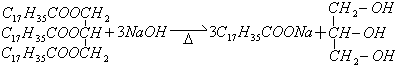 取代反应
取代反应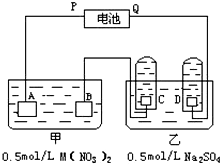 图是两种溶液进行电解的装置.电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B,C,D都是铂电极,P,Q是电池的两极,
图是两种溶液进行电解的装置.电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B,C,D都是铂电极,P,Q是电池的两极,