题目内容
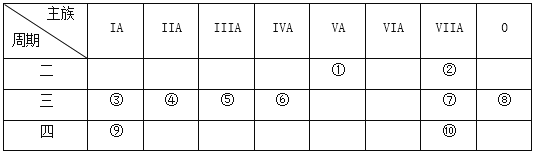
【题目】X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是________,Y的单质分子的结构式为__________,DZ的电子式为________,DZ化合物中离子半径较大的是________(填离子符号)。
(2)X元素形成的同素异形体的晶体类型可能是________(填序号)。
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):__________;Y、Z的氢化物分子结合H+能力较强的是(写化学式)________。
(4)下列可作为比较D和Na金属性强弱的依据是________。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为___________。
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由__________。
【答案】 第4周期VIII族 N≡N ![]() O2- ①、④ CH4 NH3 bd 4NH3+5O2
O2- ①、④ CH4 NH3 bd 4NH3+5O2![]() 4NO+6H2O 氢元素的最高正价和最低负价的绝对值相等(或者氢元素的最高正价与最低负价的代数和为0)
4NO+6H2O 氢元素的最高正价和最低负价的绝对值相等(或者氢元素的最高正价与最低负价的代数和为0)
【解析】E的单质在Z2中燃烧的产物可使品红溶液褪色,该气体为SO2,则E为S元素,Z为O元素,F和Z元素形成的化合物F3Z4具有磁性,则F3Z4为Fe3O4,F为Fe元素,X的单质在Z2中燃烧可生成XZ和XZ2两种气体,X原子序数小于O元素,应为CO和CO2气体,X为C元素,D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体,应为Mg和CO2的反应,则D为Mg元素,Y的原子序数介于碳、氧之间,则Y为N元素,据此解答。
根据以上分析可知X是C,Y是N,Z是O,D是Mg,E是S,F是Fe。则
(1)F为Fe元素,在周期表中的位置是第4周期第Ⅷ族,Y的单质分子为N2,结构式为N≡N,DZ为MgO,属于离子化合物,电子式为![]() 。核外电子排布相同时离子半径随原子序数的增大而减小,则DZ化合物中离子半径较大的是O2-;
。核外电子排布相同时离子半径随原子序数的增大而减小,则DZ化合物中离子半径较大的是O2-;
(2)X为碳元素,碳元素形成的同素异形体有石墨、金刚石、C60等,金刚石属于原子晶体,C60属于分子晶体,答案为:①④;
(3)C、N、O形成的10电子氢化物分别是CH4、NH3、H2O,氨气分子间存在氢键,导致氨气的沸点升高,甲烷中不含氢键,所以沸点较低的是CH4,氨气为碱性气体,NH3结合H+能力较强;
(4)a.单质的硬度和熔、沸点与金属性强弱没有关系,a错误;b.金属性越强,最高价氧化物对应水化物的碱性越强,则比较两元素最高价氧化物对应的水化物溶液的碱性强弱可以比较二者的金属性强弱,b正确;c.两种元素在氯化物中化合价的高低与金属性强弱没有关系,c错误;d.金属性越强,其单质与酸反应越剧烈,则比较单质与同浓度盐酸反应的剧烈程度可以比较金属性强弱,d正确。答案选bd;
(5)Y的氢化物氨气和Z的单质氧气在一定条件下反应生成Z的氢化物(产物之一),该反应属于氨的催化氧化,反应的方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
(6)由于氢元素的最高正价和最低负价的绝对值相等(或者氢元素的最高正价与最低负价的代数和为0),因此建议将氢元素排在元素周期表的ⅣA族。