题目内容
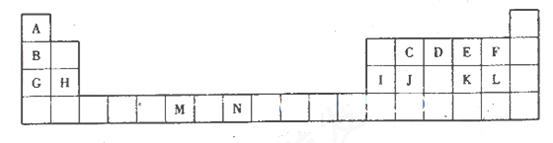
(14分)下图是元素周期表的一部分
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | | |
| ⑥ | | | | | | | | | | | | ⑦ | | | | ⑧ | |
| | | | ⑨ | | | | ⑩ | | | | | | | | | | |
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是 。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式 。
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是 (填“s”、“p”、“d”、“ds”等)区元素,位于 族;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为 。
(1)  ;14 (2)分子间存在氢键,H2O分子发生缔合
;14 (2)分子间存在氢键,H2O分子发生缔合
(3)2OH— + Be(OH)2=BeO22—+ 2H2O (4)①R 和U ② p(1分) IIIA(1分)120°
解析试题分析:(1)根据元素在周期表中的位置可知,元素⑨是钛元素,原子序数是22,因此根据核外电子排布规律其知的价电子轨道表示式为 。元素⑩是铁,其次外层电子数为14个。
。元素⑩是铁,其次外层电子数为14个。
(2)元素⑤是水,水分子间存在氢键,H2O分子发生缔合,因此测定结果比理论值高。
(3)②、⑦分别是Be和Al,氢氧化铝是两性氢氧化物,则元素②的氢氧化物与NaOH溶液反应的离子方程式为2OH— + Be(OH)2=BeO22—+ 2H2O。
(4)由元素的电离能可以看出,Q的电离能很大,可能为零族元素,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族,S的第一、第二电离能较小,第三电离能剧增,故表现+2价,最外层电子数为2,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3,则
①由上述分析可知,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族。
②由上述分析可知,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3,可能为P区元素,位于第ⅢA族;若T为第二周期元素,则T是B元素。Z是第三周期元素中原子半径最小的主族元素,因此Z是氯元素,则T、Z形成的化合物是BCl3,B原子的价层电子对数是3个,且不存在孤对电子,所以是平面三角形结构,分子键角为120°。
考点:考查元素周期表的结构、元素周期律的应用

元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑤ | | ⑥ | | |
| 3 | ① | ③ | ④ | | | | ⑦ | ⑨ |
| 4 | ② | | | | | | ⑧ | |
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是 (填化学式)。
(3)①、②、③三种元素按离子半径由大到小的顺序依次为 (填离子符号)。
(4)⑥元素形成的具有强氧化性的氢化物电子式是 , 该元素另一种氢化物在常温下与 ②发生反应的化学方程式为 。
(16分)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
| | | | |||||||||||||||
| | | | | h | | | | | |||||||||
| a | c | f | | i | | | m | ||||||||||
| | | | e | | | | | | | | | | g | | k | | |
| | d | | | | | | | | | | | | | | | | |
(1)表中所列元素中,属于短周期元素的有 (写元素符号),
e元素在元素周期表中的位置是 周期, 族。
(2)下列 组元素的单质可能都是电的良导体。
A、a, c, h B 、 i ,g, k C、c, h, m D、 d, e, f
(3)i元素属于 (填金属或非金属)元素,它的最高正化合价是
负化合价是 。它能跟氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,写出它跟氧气反应的化学方程式: 。
(16分)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如右图所示变化。己知l个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。请回答下列问题: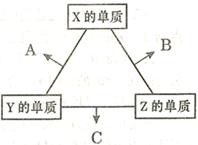
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物的化学式为 ,相同浓度上述水溶液中由水电离出的c(H+)最小的是 (填写化学式)。
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,试写出该电池负极的电极反应式 ,溶液中OH-向 极移动(填“正”或“负”)。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,该反应的化学方程式为 。
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol?L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
_____________________________________________________。
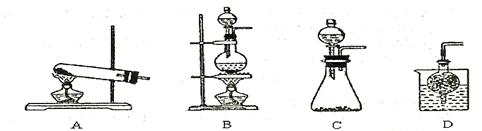
③实验室可用甲作试剂取X的单质,发生装置可选用下图中的 (填装置代号)。