题目内容
在恒容的密闭容器中,下列反应分别达到平衡后,有关说法正确的是
A.2HI(g) H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 |
B.2NO2(g) N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 |
C.2SO2(g)+O2(g) 2SO3(g);DH<0,升温后,平均相对分子质量减小 2SO3(g);DH<0,升温后,平均相对分子质量减小 |
D.3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 |
C
考查了勒夏特列原理的相关内容
A:降温,平衡正向移动,碘蒸气浓度增大,颜色加深,但气体总物质的量不变,压强不变
B:在恒容状态下,充入氩气,虽体系压强增大,但各物质的浓度不变,对反应无任何影响。
C:升温,平衡逆向移动,气体的总物质的量增大,而质量不变,故平均相对分子质量减小。
D:铁为固体,不会影响反应。
故答案为C
A:降温,平衡正向移动,碘蒸气浓度增大,颜色加深,但气体总物质的量不变,压强不变
B:在恒容状态下,充入氩气,虽体系压强增大,但各物质的浓度不变,对反应无任何影响。
C:升温,平衡逆向移动,气体的总物质的量增大,而质量不变,故平均相对分子质量减小。
D:铁为固体,不会影响反应。
故答案为C

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
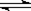 4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白: PH3(g) + HI(g) ① ;
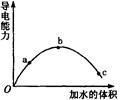
PH3(g) + HI(g) ① ; 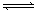 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是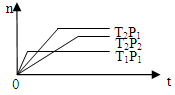
 2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。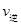 (X2)=2
(X2)=2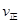 (Y2) d.容器内的密度保持不变
(Y2) d.容器内的密度保持不变 2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )
2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )
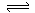 2C0(g) △H>O,K1 ①
2C0(g) △H>O,K1 ①