题目内容
室温时,M(OH)2(S) M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于
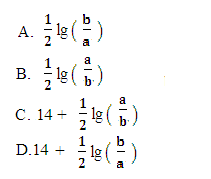
 M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于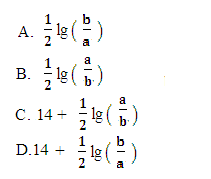
C
由Ksp=a=c2(OH-)c(M2+)得,c(OH-)=(a/b)1/2,结合Kw换算成c(H+)=10-14/(a/b)1/2,然后求pH。答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
题目内容
 M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),Ksp =a,c(M2+)=bmol·L-1时,溶液的pH等于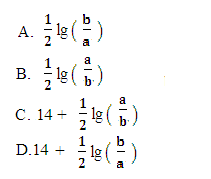

 阅读快车系列答案
阅读快车系列答案