题目内容
【题目】下列实验操作不正确的是
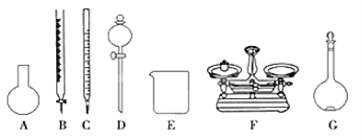
A. 分液漏斗使用前需要先检查是否漏液
B. 实验中剩余的钠不能再放回原试剂瓶
C. 做焰色反应时,铂丝应用盐酸洗净并灼烧至无色
D. 蒸馏烧瓶加热时需要垫石棉网
【答案】B
【解析】A.具有塞子、活塞的仪器使用前需要查漏,则分液漏斗使用前需要先检查是否漏液,故A正确;B.钠与水反应生成NaOH具有腐蚀性,且放热,存在安全隐患,则试验中剩余的钠,需要再放回原试剂瓶,故B错误;C.盐酸易挥发,灼烧后不干扰实验,则焰色反应时,铂丝应用盐酸洗净并灼烧至无色,故C正确;D.蒸馏烧瓶不能直接加热,则蒸馏烧瓶加热时需要垫石棉网,故D正确;故选B。

 字词句段篇系列答案
字词句段篇系列答案【题目】(12分)下表为长式周期表的一部分,其中的编号代表对应的元素。
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | [ | ⑦ | |||||||||||||
⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区元素的是 (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为________________。
(3)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑦和⑧形成的化合物的电子式为 。
(6)元素⑩的基态原子核外电子排布式是 。
(7)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
_______________________________________________。