题目内容
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:
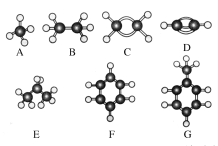
(1)常温下含碳量最高的气态烃是________(填对应字母);
(2)能够发生加成反应的烃有________(填数字)种;
(3)一卤代物种类最多的是________(填对应字母);
(4)写出实验室制取D的化学方程式________________________________;
(5)写出F发生溴代反应的化学方程式______________________________。
【答案】D 4 G CaC2+2H2O→Ca(OH)2+CH≡CH↑ C6H6 + Br2 ![]() C6H5Br + HBr
C6H5Br + HBr
【解析】
由结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,根据物质的组成、结构和性质解答该题。
由结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,
(1)依据碳氢质量比可以看出,常温下含碳量最高的气态烃是乙炔,
故答案为:D;
(2)能够发生加成的烃为不饱和烃,则有乙烯、乙炔、苯和甲苯4种,
故答案为:4;
(3)一卤代物种类最多的是甲苯,共有4种,
故答案为:G;
(4)实验室用电石与水反应制备乙炔,其化学方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑,
故答案为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(5)F为苯,与液溴在FeBr3作用下发生溴代反应,其化学方程式为:C6H6 + Br2 ![]() C6H5Br + HBr,
C6H5Br + HBr,
故答案为:C6H6 + Br2 ![]() C6H5Br + HBr。
C6H5Br + HBr。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案【题目】J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
J | ||||
R |
(1)M的离子结构示意图为__________;元素T在周期表中位于第________族。
(2)J元素名称是______,他和氢组成10电子的化合物,其分子式为______________,属___________(填“离子化合物”或“共价化合物”)。
(3)R元素符号为_______,其最高能层符号是________。
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,按要求用化学式或化学用语填空,用序号填写不得分。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_____________;
(2)地壳中含量最多的非金属元素是_____________;
(3)与水反应最剧烈的金属单质是_____________;
(4)某元素三价阳离子的核外有10个电子,该元素是_____________;
(5)气态氢化物最稳定的化合物是_____________;
(6)①的最高价氧化物的电子式为_____________;
(7)用电子式表示④和⑨形成化合物的过程_____________。
(8)最高价氧化物对应的水化物碱性最强的化合物是_____________;元素的最高价氧化物对应的水化物中具有两性的化合物是_____________;两者反应的离子方程式为_____________。
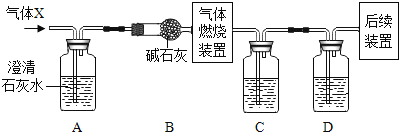
【题目】仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能实现相应实验目的的是( )
选项 | A | B | C | D |
实验目的 | 除去KCl中少量的MnO2 | 用10mol·L-1的盐酸配制100mL0.1 mol·L-1的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
实验仪器或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |
|
|
A.AB.BC.CD.D