题目内容
铋(Bi)在医药方面有重要应用。下列关于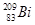 i和
i和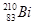 的说法正确的是
的说法正确的是
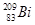 i和
i和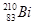 的说法正确的是
的说法正确的是A.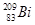 i和 i和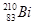 都含有83个中子 都含有83个中子 |
B.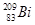 和 和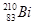 互为同位素 互为同位素 |
C.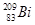 i和 i和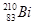 的核外电子数不同 的核外电子数不同 |
D.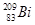 i和 i和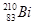 都含有83个质子,是同一种核素 都含有83个质子,是同一种核素 |
B
试题分析:在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。A、因为质子数和中子数之和是质量数,所以
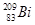 和
和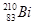 含有的中子数分别是209-83=126、210-83=128,A不正确;B、
含有的中子数分别是209-83=126、210-83=128,A不正确;B、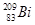 和
和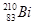 的质子数相同,但中子数不同,二者互为同位素,B正确;C、
的质子数相同,但中子数不同,二者互为同位素,B正确;C、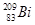 和
和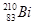 的质子数相同,由于质子数=核外电子数,所以二者的核外电子数也是相同的,C不正确;D、
的质子数相同,由于质子数=核外电子数,所以二者的核外电子数也是相同的,C不正确;D、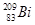 和
和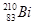 都含有83个质子,但中子数不同,属于不同种核素,D不正确,答案选B。
都含有83个质子,但中子数不同,属于不同种核素,D不正确,答案选B。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目