题目内容
下列叙述中,不能用勒夏特列原理解释的是( )
| A.合成氨需用铁触媒加快反应速率 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.收集氯气可用排饱和食盐水法 |
AC
催化剂只能改变反应速率,不难改变平衡状态,A正确。氢气和碘合成碘化氢的反应是体积不变的可逆反应,所以增大压强,平衡不移动。颜色加深是因为体积减小,浓度增大导致的,C正确。B属于压强对平衡状态的影响,C属于浓度对平衡状态的影响,均可以用勒夏特列原理来解释。答案选AC。

练习册系列答案
相关题目
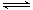 2Z(g )+ W(s) ;△H >0达到平衡,下列判断正确的是( )
2Z(g )+ W(s) ;△H >0达到平衡,下列判断正确的是( )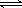 2SO3(g),下列判断不正确的是
2SO3(g),下列判断不正确的是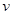 正(O2)=
正(O2)=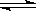 2HF
2HF 
 SO2Cl2(l) △H=—97.3kJ/mol
SO2Cl2(l) △H=—97.3kJ/mol C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到该条件下的最大限度的是 H2(气)+I2(气),达到平衡时,下列说法正确的是 ( )
H2(气)+I2(气),达到平衡时,下列说法正确的是 ( ) PCl3(g)+Cl2(g);△H1>0 K1=1mol·L—1
PCl3(g)+Cl2(g);△H1>0 K1=1mol·L—1