题目内容
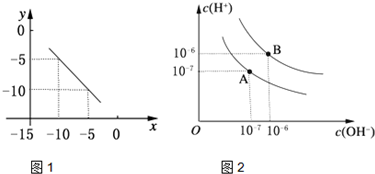
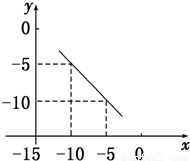
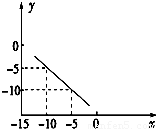
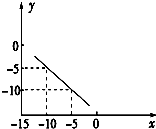 在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.
在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.(1)该温度下,0.01mol?L-1NaOH溶液的pH为
13
13
.(2)在此温度下,将pH=13的NaOH溶液Va L与pH=1的硫酸溶液Vb L混合.
①若所得混合液为中性,则Va:Vb=
10:1
10:1
.②若所得混合液的pH=2,则Va:Vb=
9:2
9:2
.分析:(1)由图可知,x=-5时,y=-10,x=-10时,y=-5,则该温度下,Kw=10-15,0.01mol?L-1NaOH溶液中c(OH-)=10-2mol?L-1,以此计算;
(2)①所得混合液为中性,则Va L×0.01mol/L=Vb L×0.1mol/L;
②若所得混合液的pH=2,则
=0.01mol/L.
(2)①所得混合液为中性,则Va L×0.01mol/L=Vb L×0.1mol/L;
②若所得混合液的pH=2,则
| Vb L×0.1mol/L-Va L×0.01mol/L |
| Va+Vb |
解答:解:(1)由图可知,x=-5时,y=-10,x=-10时,y=-5,则该温度下,Kw=10-15,0.01mol?L-1NaOH溶液中c(OH-)=10-2mol?L-1,则c(H+)=10-13mol?L-1,所以pH=13,
故答案为:13;
(2)①所得混合液为中性,则Va L×0.01mol/L=Vb L×0.1mol/L,解得Va:Vb=10:1,故答案为:10:1;
②若所得混合液的pH=2,即酸过量,则
=0.01mol/L,解得Va:Vb=9:2,故答案为:9:2.
故答案为:13;
(2)①所得混合液为中性,则Va L×0.01mol/L=Vb L×0.1mol/L,解得Va:Vb=10:1,故答案为:10:1;
②若所得混合液的pH=2,即酸过量,则
| Vb L×0.1mol/L-Va L×0.01mol/L |
| Va+Vb |
点评:本题考查酸碱混合pH的计算,由图象得出该温度下的Kw是解答本题的关键,并注意酸碱混合氢离子与氢氧根离子的关系来计算,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
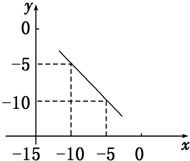 在某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示:
在某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示: