��Ŀ����
13��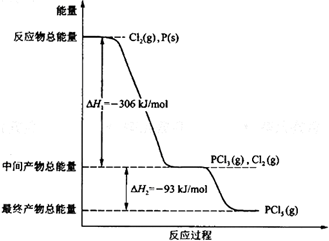 ����P��s����Cl2��g��������Ӧ����PCl3��g����PCl5��g������Ӧ���̺�������ϵ��ͼʾ��ͼ�еġ�H��ʾ����1mol��������ݣ���
����P��s����Cl2��g��������Ӧ����PCl3��g����PCl5��g������Ӧ���̺�������ϵ��ͼʾ��ͼ�еġ�H��ʾ����1mol��������ݣ���������ͼ�ش��������⣺
��1��P��Cl2��Ӧ����PCl3���Ȼ�ѧ����ʽ��
P��s��+$\frac{3}{2}$Cl2��g���TPCl3��g������H=-306kJ•mol-1��
��2��PCl5�ֽ��PCl3��Cl2���Ȼ�ѧ����ʽ��
PCl5��g��=PCl3��g��+Cl2��g������H=+93 kJ/mol��
�����ֽⷴӦ��һ�����淴Ӧ���¶�T1ʱ�����ܱ������м���0.80mol Pol5����Ӧ��ƽ��ʱ��PCl5��ʣ0.60mol����ֽ��ʦ�1����25%������Ӧ�¶���T1���ߵ�T2��ƽ��ʱPCl5�ķֽ���Ϊ��2����2���ڦ�1������ڡ�����С�ڡ����ڡ�����
��3����ҵ���Ʊ�PCl5ͨ�����������У��Ƚ�P��Cl2��Ӧ�����м����PCl3��Ȼ���£��ٺ�Cl2��Ӧ����PCl5��ԭ����������Ӧ��Ϊ���ȷ�Ӧ�������¶���������߲��ʣ���ֹ����ֽ�
��4��P��Cl2��������Ӧ����1mol PCl5�ġ�H3=-399kJ•mol-1
��5��P��Cl2һ����Ӧ����1mol PCl5�ġ�H4���ڡ�H3������ڡ�����С�ڡ����ڡ�����PCl5������ˮ��ַ�Ӧ���������������ᣬ�仯ѧ����ʽ��PCl5+4H2O�TH3PO4+5HCl��
���� ��1���Ȼ�ѧ����ʽ��дҪ��ע�������ʵľۼ�״̬���жϷ��ȷ�Ӧ�������ȷ�Ӧ����Ӧ������ʵ����뷴Ӧ�ȳɶ�Ӧ�ı�����ϵ������ͼʾP��s��+Cl2��g����PCl3��g������Ӧ�����������������������������÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��Ϊ��H=-306 kJ/mol���ɴ˷������
��2������H=������������-��Ӧ����������Cl2��g��+PCl3��g��=PCl5��g�����м������������������ղ�������������÷�Ӧ�Ƿ��ȷ�Ӧ������ PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ���Ȼ�ѧ����ʽ��PCl5��g��=PCl3��g��+Cl2��g������H=+93 kJ/mol��
PCl5�ֽ��ʦ�1=$\frac{0.8mol-0.6mol}{0.8mol}$��100%=25%��PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ�������¶������ȷ�Ӧ�����ƶ�������Ӧ���ֽⷴӦ�����ȷ�Ӧ�������ȷ�Ӧ�������¶�������Ӧ�����ƶ���Ȼ��ó��ֽ��ʴ�С��
��3��Cl2��g��+PCl3��g��=PCl5��g�����Ƿ��ȷ�Ӧ������ƽ������ȷ�Ӧ�����ƶ���
��4�����ݸ�˹���ɷ�����
��5�����ݸ�˹���ɿ�֪����Ӧ����һ����ɻ��Ƿֶಽ��ɣ�������ͬ�IJ����Ӧ����ȣ���P��Cl2һ����Ӧ����1molPCl5�ķ�Ӧ�ȵ���P��Cl2��������Ӧ����1molPCl5�ķ�Ӧ�ȣ�PCl5������ˮ��ַ�Ӧ������������������ᣮ
��� �⣺��1���Ȼ�ѧ����ʽ��дҪ��ע�������ʵľۼ�״̬���жϷ��ȷ�Ӧ�������ȷ�Ӧ����Ӧ������ʵ����뷴Ӧ�ȳɶ�Ӧ�ı�����ϵ������ͼʾP��s��+Cl2��g����PCl3��g������Ӧ�����������������������������÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ��Ϊ��H=-306 kJ/mol���Ȼ�ѧ����ʽΪ��P��s��+$\frac{3}{2}$Cl2��g���TPCl3��g������H=-306 kJ/mol��
�ʴ�Ϊ��P��s��+$\frac{3}{2}$Cl2��g���TPCl3��g������H=-306kJ•mol-1��
��2����H=������������-��Ӧ����������Cl2��g��+PCl3��g��=PCl5��g�����м������������������ղ�������������÷�Ӧ�Ƿ��ȷ�Ӧ������ PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ���Ȼ�ѧ����ʽ��PCl5��g��=PCl3��g��+Cl2��g������H=+93 kJ/mol��
PCl5�ֽ��ʦ�1=$\frac{0.8mol-0.6mol}{0.8mol}$��100%=25%��PCl5��g��=PCl3��g��+Cl2��g�������ȷ�Ӧ�������¶������ȷ�Ӧ�����ƶ�������Ӧ���ֽⷴӦ�����ȷ�Ӧ�������ȷ�Ӧ�������¶�������Ӧ�����ƶ���ת��������2 ����1 ��
�ʴ�Ϊ��PCl5��g���TPCl3��g��+Cl2��g������H=+93kJ•mol-1��25%�����ڣ�
��3��Cl2��g��+PCl3��g��=PCl5��g�����Ƿ��ȷ�Ӧ������ƽ������ȷ�Ӧ�����ƶ�������������PCl5��g�������ɣ�
�ʴ�Ϊ��������Ӧ��Ϊ���ȷ�Ӧ�������¶���������߲��ʣ���ֹ����ֽ⣻
��4�����ݸ�˹���ɣ�P��Cl2��������Ӧ��һ����Ӧ����PCl5�ġ�HӦ������ȵģ�P��Cl2��������Ӧ����1 molPCl5���Ȼ�ѧ����ʽ��
P��s��+$\frac{3}{2}$Cl2��g��=PCl3��g������H1=-306 kJ/mol��
Cl2��g��+PCl3��g��=PCl5��g������H2=-93 kJ/mol��
P��Cl2һ����Ӧ����1molPCl5�ġ�H3=-306 kJ/mol+��-93 kJ/mol��=-399 kJ/mol��
�ʴ�Ϊ��-399kJ•mol-1��
��5�����ݸ�˹���ɿ�֪����Ӧ����һ����ɻ��Ƿֶಽ��ɣ�������ͬ�IJ����Ӧ����ȣ���P��Cl2һ����Ӧ����1molPCl5�ķ�Ӧ�ȵ���P��Cl2��������Ӧ����1molPCl5�ķ�Ӧ�ȣ�PCl5������ˮ��ַ�Ӧ�����������������������ᣬ��ԭ���غ��֪��ѧ����ʽΪPCl5+4H2O�TH3PO4+5HCl��
�ʴ�Ϊ�����ڣ�PCl5+4H2O�TH3PO4+5HCl��
���� ���⿼���Ȼ�ѧ����ʽ����д����ѧƽ����㡢��������Ի�ѧƽ���ƶ���Ӱ�켰��Ӧ�ȵļ����֪ʶ����������ע�⣺�Ȼ�ѧ����ʽ��û�б�ע�����ʵľۼ�״̬�������ʵ����ʵ����뷴Ӧ��û�г��ֶ�Ӧ�ı�����ϵ��������ȷ�жϷ��ȷ�Ӧ�����ȷ�Ӧ��

| A�� | CH2=CH2 | B�� | SO2 | C�� |  | D�� | CH3CH3 |
| A�� | 0.1b/a mol•L-1 | B�� | 1��10-1 mol•L-1 | ||
| C�� | 1��10-7 mol•L-1 | D�� | 0.1b/��a+b�� mol•L-1 |
��H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H1
��$\frac{1}{2}$N2��g��+O2��g���TNO2��g����H2
��$\frac{1}{2}$N2��g��+$\frac{3}{2}$H2��g���TNH3��g����H3
��ô����ͬ�¶��·�Ӧ��4NH3��g��+7O2��g���T4NO2��g��+6H2O��g�����ʱ�Ϊ��������
| A�� | 4��H3-6��H1-4��H2 | B�� | 6��H1+4��H2-4��H3 | C�� | ��H1+��H2-��H3 | D�� | ��H3-��H1-��H2 |
 �����ʵ����ĸ����ʷֱ���������Na��NaOH������Cu��OH��2��Ӧ�������������ʵ����ʵ���֮��Ϊ��������
�����ʵ����ĸ����ʷֱ���������Na��NaOH������Cu��OH��2��Ӧ�������������ʵ����ʵ���֮��Ϊ��������| A�� | 6��4��5 | B�� | 1��1��1 | C�� | 3��2��2 | D�� | 3��2��3 |
| A�� | 2��2-���������2-�����黥Ϊͬ���칹�� | |
| B�� | �е㣺�����飾�����飾2-������ | |
| C�� | ����ʽ�ֱ�ΪC5H12��C9H20��C100H202���л���һ����Ϊͬϵ�� | |
| D�� | ����5��̼ԭ�ӵ���������ͬ���칹�� |
| A�� | H2O2 | B�� | Na2O2 | C�� | H2S | D�� | Mg��NO3��2 |
 ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ������ᣬD�з��б���̼������Һ����ش�
ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A�з���Ũ���ᣬB�з����Ҵ������ᣬD�з��б���̼������Һ����ش� CH3CO18OC2H5+H2O��
CH3CO18OC2H5+H2O��