籾朕坪否
和双並糞音嬬傍苧掲署奉來Cl﹅I議頁↙ ⇄。
A. Cl2+2I-==2Cl-+I2 B. 糧協來⦿HCl﹅HI
C. 磨來⦿HClO4﹅HIO4 D. 磨來⦿HClO3﹅HIO3
根紀議晒栽麗鴻刑贋壓噐徭隼順⇧頁匯窃掲械嶷勣議晒栽麗。指基和双嗤購諒籾⦿

↙1⇄壓匯協訳周和⦿2N2(g)+6H2O(g)=4NH3(g)+3O2(g)。厮岑乎郡哘議屢購議晒僥囚囚嬬方象泌和⦿
晒僥囚 | N《N | H-O | N-H | O=O |
E/↙kJ/mol⇄ | 946 | 463 | 391 | 496 |
夸乎郡哘議ΔH=_______________kJ/mol。
↙2⇄壓冴否畜液否匂嶄割秘2molNO2嚥1molO2窟伏郡哘泌和⦿
4NO2(g)+O2(g)  2N2O5(g)
2N2O5(g)
〙厮岑壓音揖梁業和霞誼N2O5議麗嵎議楚昧扮寂議延晒泌夕1侭幣。械梁和⇧乎郡哘嬬剃﨑徭窟序佩⇧圻咀頁_______________________。
〖和双嗤購乎郡哘議傍隈屎鳩議頁___________。
A⤴制寄否匂悶持⇧峠財﨑剃郡哘圭﨑卞強⇧詞栽賑悶冲弼延侮
B⤴冴梁冴否⇧壅割秘2molNO2才1molO2⇧壅肝器欺峠財扮NO2廬晒楕奐寄
C⤴冴梁冴否⇧輝否匂坪議畜業音壅個延⇧夸郡哘器欺峠財彜蓑
D⤴飛乎郡哘議峠財械方奐寄⇧夸匯協頁週詰阻梁業
↙3⇄N2O5頁匯嶽仟侏駄弼嵓晒質⇧凪崙姥辛參喘盗狽晒墜伴創窮学恬窮坿⇧寡喘窮盾隈崙姥誼欺N2O5⇧垢恬圻尖泌夕。夸盗狽晒墜伴創窮学議減自郡哘塀葎 _________________________。

0.01 mol/L 議卑匣 | X | Y | Z | W |
pH | 12 | 2 | 8.5 | 4.5 |
X、Y、Z、W蛍艶頁HNO3、NH4NO3、NaOH、NaNO2膨嶽膿窮盾嵎嶄議匯嶽。貧燕頁械梁和敵業譲葎0.01 mol/L議X、Y、Z、W卑匣議pH。繍X、Y、Z光1mol揖扮卑噐邦嶄誼欺詞栽卑匣⇧夸詞栽卑匣嶄光宣徨議敵業喇寄欺弌議乏會葎_______________________。
紀議剳晒麗嚥傅検壓寄賑嶄議今冦腺徨屢札恬喘扮⇧膚式泌和郡哘⦿
↔⦿2NO2(g)+ NaCl(s) NaNO3(s)+ ClNO(g) K1
NaNO3(s)+ ClNO(g) K1
Å⦿2NO(g)+ Cl2(g) 2ClNO(g) K2
2ClNO(g) K2
〙4NO2(g)+ 2NaCl(s) 2NaNO3(s)+ 2NO(g)+Cl2(g)議峠財械方K=_________↙喘K1、K2燕幣⇄
2NaNO3(s)+ 2NO(g)+Cl2(g)議峠財械方K=_________↙喘K1、K2燕幣⇄
〖壓冴梁訳周和⇧﨑2L冴否畜液否匂嶄紗秘0.2molNO才0.1molCl2⇧10min扮郡哘Å器欺峠財。霞誼10min坪v(ClNO)=7.5〜10-3mol/(L,min)⇧夸峠財扮NO議廬晒楕α1=___________◉凪麿訳周音延⇧郡哘Å壓冴儿訳周和序佩⇧峠財扮NO議廬晒楕α2________α1↙野^﹅ ̄ ^〽 ̄賜^﹆ ̄⇄


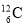 、
、 、
、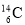 ⇧和双光𡸴斤眉嶽圻徨譲音揖議頁
⇧和双光𡸴斤眉嶽圻徨譲音揖議頁 奐寄
奐寄