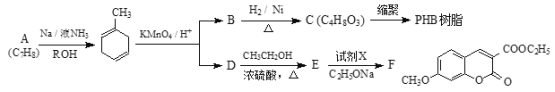
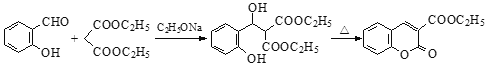
题目内容
【题目】某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法产生了兴趣。
探究一 菠菜里是否含有可溶性草酸盐和碳酸盐?
【查阅资料】
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。
②醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。
【实验流程】
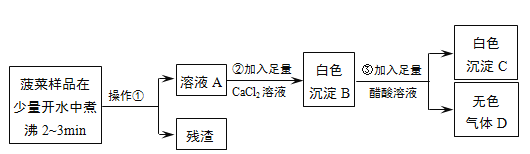
根据流程回答问题:(1)操作①是_________。 ( 2)加入足量CaCl2溶液的目的是_________。
(3)已知气体D能使澄清石灰水变浑浊,步骤③的化学反应方程式为_________。
【实验结论】菠菜里含有可溶性草酸盐和碳酸盐。
探究二 人体结石的主要成分是草酸钙,草酸钙高温分解的产物是什么?
【查阅资料】
① 草酸钙高温完全分解得到两种气态氧化物和一种固态氧化物。
② 12.8 g的草酸钙分解过程中温度与剩余固体的质量关系如下图所示。
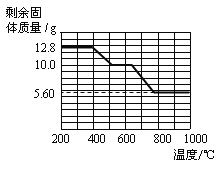
【实验分析】(4)草酸钙高温完全分解的化学方程式为_____________。
(5)通过上图数据分析,700℃时剩余固体的成分是_____________。
(6)请你设计实验,验证700℃时剩余固体的成分。
实验操作 | 实验现象 | 实验结论 |
【答案】探究一:(1)过滤(2)将溶液中的草酸根和碳酸根完全沉淀出来
(3)CaCO3 + 2HAc=Ca(Ac)2 + H2O + CO2↑
探究二:(1)CaC2O4![]() CaO + CO↑+ CO2↑(2)CaCO3和CaO
CaO + CO↑+ CO2↑(2)CaCO3和CaO
实验操作 | 实验现象 | 实验结论 |
取少量固体于试管中,加入适量的水,用手触摸试管壁;静置后取上层清液,滴加无色酚酞试液。 取不溶物于试管中,加入足量的稀盐酸,将气体通入澄清石灰水。 | 试管壁发烫, 溶液变红 有气泡冒出,澄清石灰水变浑浊。 | 该固体中含有CaO。 该固体中含有CaCO3。 剩余固体的成分为CaO和CaCO3 |
【解析】
试题分析:探究一:(1)分离固态和可溶性物质的一种常用方法------过滤,本题操作①之后是残渣和溶液,故我们判断该操作为过滤;
(2)由于我们探究的是菠菜中的两种盐,由题给条件可知,有一种可溶,一种不可溶,所以我们想办法将溶液中的草酸根和碳酸根完全沉淀出来,而氯化钙可以把它们都给沉淀出来,然后根据“醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐”这一结论来完成它们的判定;
(3)根据题给条件,反应生成了使澄清石灰水变浑浊的气体,再结合题给信息我们可以判断发生的反应为:CaCO3+2HAc=Ca(Ac)2+H2O+CO2↑;
探究二:(1)根据题给条件及质量守恒定律可知,草酸钙中含有钙元素、碳元素、和氧元素,那么生成的气态氧化物就是一氧化碳和二氧化碳,从而可以写出该化学方程式为CaC2O4![]() CaO + CO↑+ CO2↑;
CaO + CO↑+ CO2↑;
(2)从图表中可以分析出,草酸钙的分解分为两个过程,再结合题给条件可知第一个过程中生成的应该是一氧化碳和碳酸钙,然后碳酸钙分解产生二氧化碳,在700℃时正处在碳酸钙分解的过程中,故剩余的固体成分为碳酸钙和氧化钙的混合物,要验证碳酸钙和氧化钙可以根据这两种物质的性质,分别检验,其中碳酸钙可以和盐酸反应生成二氧化碳,氧化钙可以水反应生成碱,同时放出大量的热;