题目内容
NA表示阿伏加德罗常数,下列叙述正确的是
A. 1molFeI2与足量氯气反应时转移的电子数为2NA
B. 2L 0.5mol·L-1硫酸钾溶液中阴离子所带电荷数为NA
C. 把1mL 1 mol·L-1 FeCl3滴入到沸水中,加热一段时间,直至溶液变为红褐色,得到Fe(OH)3 胶体数为0.001NA
D. 丙烯与环丙烷组成的42g混合气体中氢原子的个数为6NA
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
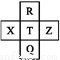
天天向上课时同步训练系列答案如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ⑧ | ⑨ | ② | ③ | ||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)③、④、⑦的原子半径由大到小的顺序是_________(用元素符号表示)。
(2)下列事实能说明②元素的非金属性比⑥元素的非金属性强的是__________。
a.②的单质与⑥元素的简单氢化物溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol②单质比1mol⑥单质得电子多
c.②和⑥两元素的简单氢化物受热分解,前者的分解温度高。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+ 氧化,写出该反应的离子方程式 ___________________。
(4) 已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式 _______________________。
(5)已知W+X=Y+Z(反应需要加热,),W、X、Y、Z分别是由①②⑨三种元素形成的四种10电子粒子(W、X为离子,Y、Z为分子),写出该化学方程式_________________。
(6)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体, D溶液显碱性。
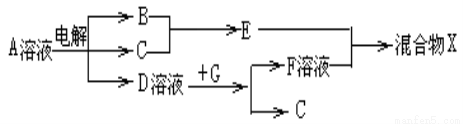
①写出D溶液与G反应的离子方程式______________________。
②写出检验A溶液中溶质的阴离子的方法____________________。
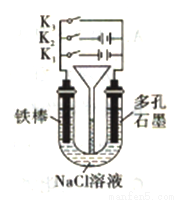
③常温下,若电解1L0.1mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为:________________。




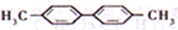 的一氯代物有5种
的一氯代物有5种