题目内容
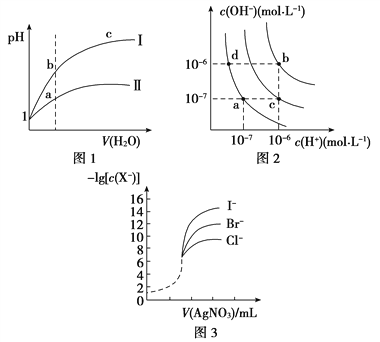
【题目】在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)![]() xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)

A.P3>P4,y轴表示C的转化率
B.P3<P4,y轴表示B的体积分数
C.P3<P4,y轴表示混合气体的密度
D.P3>P4,y轴表示混合气体的平均摩尔质量
【答案】D
【解析】
根据图1推出T1>T2,P2>P1,根据勒夏特列原理增大压强C的体积分数增大,平衡正向移动,因此正反应是体积减小的可逆反应,则x=1。升高温度C的体积分数减小,说明升高温度平衡逆向移动,则正反应放热,即△H<0。
A、随着温度升高,平衡向逆反应方向进行,C的转化率应增大,与图像不符,故A错误;
B、随着温度升高,平衡向逆反应方向进行,B的体积分数增大,与图像不符,故B错误;
C、ρ=m/V,组分都是气体,质量不变,容积是恒容,V不变,因此密度始终不变,故C错误;
D、M=m/n,组分都是气体,气体的质量不变,随着温度升高,平衡向逆反应方向进行,n增大,M减小,作等温线,随着压强的增大,平衡向正反应方向进行,n减小,M增大,符合图像,故D正确。
答案选D。

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目