题目内容
【题目】I.下列物质:①16O和18O ②红磷和白磷 ③CH3CH3和CH3CH2CH2CH3 ④CH3CH2CH2CH3 和CH3CH (CH3) 2 ⑤O2和O3 ⑥ 和
和
(1)属于同素异形体的是(填序号,下同)_______,
(2)属于同系物的是_____________。
II.乙烯的产量可以用来衡量一个国家的石油化工发展水平.请回答:
(1)乙烯的结构式是___________.
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为______.
(3)可以用来除去乙烷中混有的乙烯的试剂是______.(填序号)
①水 ②氢气 ③溴水 ④酸性高锰酸钾溶液
(4)在一定条件下,乙烯能与水反应生成有机物A,A的结构简式是______,其反应类型是______反应(填“取代”或“加成”).
(5)下列化学反应原理相同的是______(填序号).
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②SO2使溴水和酸性高锰酸钾溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
Ⅲ.如图所示为CH4燃料电池的装置(A、B为多孔碳棒):

(1)_____(填A或B)处电极入口通甲烷,其电极反应式为______________;
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为_______g。
IV.铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极的电极反应为____________________。
【答案】 ②⑤ ③ ![]() . CH2=CH2+Br2→CH2Br﹣CH2Br ③ CH3CH2OH 加成 ② B CH4+10OH--8e-===CO32-+7H2O 56 PbO2+2e-+SO42-+4H+=PbSO4+2H2O
. CH2=CH2+Br2→CH2Br﹣CH2Br ③ CH3CH2OH 加成 ② B CH4+10OH--8e-===CO32-+7H2O 56 PbO2+2e-+SO42-+4H+=PbSO4+2H2O
【解析】I.①16O和18O质子数相同,中子数不同,均属于氧元素的原子,互为同位素;②红磷和白磷均是P元素形成的不同种单质,互为同素异形体;③CH3CH3和CH3CH2CH2CH3 结构相似,分子组成上相差1个CH2原子团,属于同系物;④CH3CH2CH2CH3和CH3CH(CH3)2 分子式相同,结构不同,属于同分异构体;⑤O2和O3 均是氧元素形成的不同单质,互为同素异形体;⑥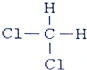 和
和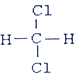 属于同种物质。
属于同种物质。
(1)属于同素异形体的为:②⑤,故答案为:②⑤;
(2)属于同系物的是③,故答案为:③;
II.(1)乙烯中C、C之间存在双键,且该分子中所有原子共面,其结构式为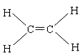 ,故答案为:
,故答案为: ;
;
(2)乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为C2H4+Br2→CH2 BrCH2Br.故答案为:C2H4+Br2→CH2 BrCH2Br
(3)①乙烯不溶于水,无法除去乙烯,故错误;②利用氢气与乙烯发生加成反应,除去乙烯,单会引入氢气,故错误;③乙烯与溴水发生加成反应生成1,2-二溴乙烷,乙烷不反应,可以除去乙烯,故正确;④酸性高锰酸钾溶液氧化乙烯,会产生二氧化碳气体,引入新杂质,故错误;故选:③;
(4)乙烯能与水发生加成反应CH2=CH2+H2O![]() CH3CH2OH,有机物A的结构简式为CH3CH2OH,故答案为:CH3CH2OH;加成;
CH3CH2OH,有机物A的结构简式为CH3CH2OH,故答案为:CH3CH2OH;加成;
(5)①乙烯使溴的四氯化碳溶液褪色是发生了加成反应,使酸性高锰酸钾溶液褪色是发生了氧化反应,原理不同,错误;②SO2使溴水和酸性高锰酸钾溶液褪色都是发生了氧化反应,原理相同,正确;③SO2使品红溶液褪色体现了二氧化硫的漂白性,使滴有酚酞的NaOH溶液褪色体现了二氧化硫的酸性氧化物的性质,原理不同,错误;故选②;
Ⅲ. (1)根据电子流向知,B为负极、A为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,所以B处通入甲烷,甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4-8e-+10OH-═CO32-+7H2O,故答案为:B;CH4-8e-+10OH-═CO32-+7H2O;
(2)由CH4+2O2+2KOH═K2CO3+3H2O知,消耗KOH的物质的量为甲烷物质的量的2倍,所以消耗氢氧化钾的物质的量是2×![]() =1mol,所以质量为:1mol×56g/mol=56g,故答案为:56;
=1mol,所以质量为:1mol×56g/mol=56g,故答案为:56;
IV. 铅失电子化合价升高而作负极,发生氧化反应,电极反应式为:Pb-2e-+SO42-=PbSO4,PbO2得电子化合价降低而作正极极,发生还原反应,电极反应式为PbO2+2e-+SO42-+4H+=PbSO4+2H2O,故答案为:PbO2+2e-+SO42-+4H+=PbSO4+2H2O。

 口算能手系列答案
口算能手系列答案【题目】除去下列物质中少量杂质(括号内杂质),所选用的试剂和分离方法达到实验目的的是
选项 | 混合物 | 试剂 | 分离方法 |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
C | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
D | 溴苯(溴单质) | 苯 | 萃取 |
A. A B. B C. C D. D
【题目】保护环境已成为当前和未来的一项全球性重大课题.为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图所示:

过程I可用如下反应表示:
①2CO2![]() 2CO+O2
2CO+O2
②2H2O![]() 2H2+O2
2H2+O2
③2N2+6H2O![]() 4NH3+3O2
4NH3+3O2
④2CO2+4H2O![]() 2CH3OH+3O2
2CH3OH+3O2
⑤2CO+H2O![]() +3O2
+3O2
请回答下列问题:
(1)过程I的能量转化形式为: 能转化为 能.
(2)请完成第⑤个反应的化学方程式
(3)上述转化过程中,△H1和△H2的关系是
(4)断裂1mol化学键所需的能量见表:
共价键 | H﹣N | H﹣O | N≡N | O=O |
断裂1mol化学键所需能量/kJmol﹣1 | 393 | 460 | 941 | 499 |
常温下,N2和H2O反应生成NH3的热化学方程式为
