题目内容
【题目】1943 年,爱国实业家侯德榜发明了“联合制碱法”,以下是联合制碱法的简单流程:

(1)纯碱固体是______(填“离子”、“分子”或“原子”)晶体。组成该物质的元素原子的半径从大到小依次为______________________。
(2)写出反应(1)的化学反应方程式_____________________。
(3)操作 X 的名称________。
(4)产品 A 的化学式是________,由溶液 B 得到产品 A,需要在溶液 B 中通入 NH3、冷冻、加食盐,其中通入 NH3 的作用是______________________;
(5)工业生产的纯碱常会含少量 NaCl 杂质。现用重量法测定其纯度,步骤如下:
①称取样品 a(g),加水溶解;
②加入足量的 BaCl2 溶液;
③过滤、_______、烘干、_______、称量。
④____________,最终得到固体 b(g)。
补全上述实验步骤;样品中纯碱的质量分数为_____________(用含 a、b 的代数式表示)。
【答案】 离子 Na>C>O CO2+H2O+NaCl+NH3→ NaHCO3↓+NH4Cl 过滤 NH4Cl 增大 NH4+ 的浓度,使 NH4Cl 更多地析出;使 NaHCO3 转化为溶解度更大的 Na2CO3,提高析出的 NH4Cl纯度 洗涤 冷却 恒重操作 ![]()
【解析】(1)纯碱是碳酸钠,其固体是离子晶体。同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则组成该物质的元素原子的半径从大到小依次为Na>C>O。(2)反应(1)生成碳酸氢钠和氯化铵,反应的化学反应方程式为CO2+H2O+NaCl+NH3→NaHCO3↓+NH4Cl。(3)将固体和溶液分离的操作名称是过滤。(4)过滤后得到碳酸氢钠,溶液中含有氯化铵。处理后得到NH4Cl;由溶液 B 得到产品 A,氨气溶于水显碱性,则通入NH3的作用是增大NH4+的浓度,使NH4Cl更多地析出;其次使NaHCO3转化为溶解度更大的Na2CO3,提高析出的NH4Cl纯度;(5)③过滤后需要洗涤,烘干后需要冷却,最后称量。④恒重操作最终得到固体 b(g),即碳酸钡是bg,所以样品中纯碱的质量分数为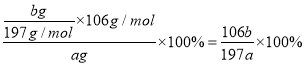 。
。





