题目内容
【题目】在实验室中严禁打闹,某几个同学在做实验中打闹而同时把盛有浓盐酸和盛固体KClO3的试剂瓶打破,使其在地上混合立即产生大量黄绿色气体,发生反应的化学方程式为:
KClO3+6HCl(浓) ![]() KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
(1)该反应中的氧化剂是 .
(2)在化学方程式上标出电子转移的方向和数目 .
(3)如反应中转移了0.50mol电子,则产生的气体在标准状况下体积为L.
(4)在清除碎片时某同学用湿毛巾捂住鼻子防止中毒,有以下四种溶液可浸湿毛巾,它们分别是:①NaOH溶液 ②NaCl溶液 ③KBr溶液 ④NaHCO3溶液.正确选择是(填试剂号数)
【答案】
(1)KClO3
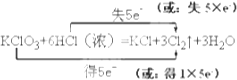
(2)
(3)6.72
(4)④
【解析】解:(1)KClO3中Cl元素的化合价降低,则KClO3为氧化剂,所以答案是:KClO3;(2)Cl元素的化合价由+5价降低为0,由﹣1价升高为0,该反应中转移5e﹣ , 电子转移的方向和数目为 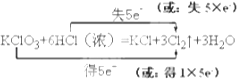 ,所以答案是:
,所以答案是: 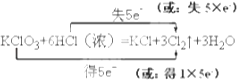 ;(3)由反应可知,转移5mol电子,生成3molCl2 , 如反应中转移了0.50mol电子,则产生的气体在标准状况下体积为0.3mol×22.4L/mol=6.72L,所以答案是:6.72;(4)用湿毛巾捂住鼻子防止中毒,应选弱碱性物质吸收氯气,只有④符合,而①碱性太强,②抑制氯气溶解,③反应生成有毒物质溴,
;(3)由反应可知,转移5mol电子,生成3molCl2 , 如反应中转移了0.50mol电子,则产生的气体在标准状况下体积为0.3mol×22.4L/mol=6.72L,所以答案是:6.72;(4)用湿毛巾捂住鼻子防止中毒,应选弱碱性物质吸收氯气,只有④符合,而①碱性太强,②抑制氯气溶解,③反应生成有毒物质溴,
所以答案是:④.

练习册系列答案
相关题目