题目内容
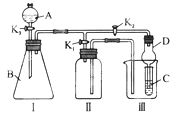
【题目】为了预防碘缺乏病,有关部门规定食盐中的碘含量(以I计)应在20~50mg/kg。制备KIO3的方法如下:
方法1:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,KH(IO3)2+KOH=2KIO3+H2O
方法2:碱性条件下,KI+3H2O ![]() KIO3+3H2↑
KIO3+3H2↑
方法3:I2![]() HIO3
HIO3![]() KIO3
KIO3
(1)与方法3相比方法1的不足是 ,
方法2的不足是。
(2)方法2选用的电极是惰性电极,则其阳极反应式是?
(3)方法3反应温度控制在70 ℃左右,不采用更高温度的主要原因是?
(4)制备纯净KIO3的实验步骤中,最后需将所得晶体最好使用洗涤2~3次,干燥后得产品。
【答案】
(1)方法1生成氯气有污染;方法2消耗大量电能
(2)
I-+6OH--6e-=IO+3H2O
(3)
H2O2分解,I2升华(答到两个要点给满分)
(4)冰水或无水乙醇(或乙醚与乙醇混合液等)
【解析】方法1有氯气产生,会造成环境污染,方法2需消耗电能;方法2选用惰性电极时,阳极I-放电,反应式为I-+6OH--6e-=IO+3H2O;方法3中的I2有升华现象,H2O2受热易分解,故应控制反应温度;制备纯净的KIO3晶体涉及的实验操作有蒸发结晶、过滤、洗涤、干燥等,洗涤时为降低KIO3的溶解度,最好使用冰水或无水乙醇等。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中.②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2﹣3次后,向其中注入0.1000molL﹣1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
滴定次数 | 待测液体积(mL) | 标准盐酸体积/mL | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.00 |
试回答下列问题:
(1)步骤③中锥形瓶中的溶液的颜色变化是由色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察 .
(3)该小组在步骤①中的错误是 , 由此造成的测定结果(填“偏高”、“偏低”或“无影响”).
(4)步骤②缺少的操作是 .
(5)如图,是某次滴定时的滴定管中的液面,其读数为mL.![]()
请计算待测烧碱溶液的浓度:mol/L.
【题目】农科院研究员在指导农民生产的过程中发现一位农民种植的某块农田小麦产量总是比邻近地块的低。他怀疑该农田可能是缺少某种元素,为此将该块肥力均匀的农田分成面积相等的五小块,进行田间试验。除施肥不同外,其他田间处理措施相同,试验结果如下表:从表中可判断,该农田最可能缺少的元素是
地块 | 甲 | 乙 | 丙 | 丁 | 戊 |
施肥情况 | 尿素 | 磷酸二氢钾 | 磷酸二氢铵 | 硫酸铵 | 不施肥 |
小麦收获量 | 55.56 | 65.26 | 56.88 | 55.44 | 55.11 |
A.NB.K
C.PD.S