题目内容
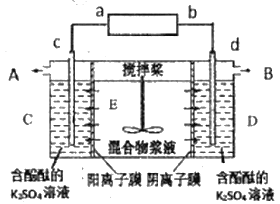
【题目】某混合物浆液中含有Al(OH)3、CuO和少量K2Cr2O7,为了得到含铬元素的溶液,常采用电解法,装置如图。a和b为电源的两极,c和d为石墨电极,A和B是电解产物,电解过程中C极室无色溶液变红。下列说法错误的是( )
A.D室发生反应为:2H2O-4e-=4H++O2↑,得到含铬元素溶液,含铬元素的微粒是Cr2O72-
B.浆液中K+移向C室,C室产物是KOH和H2
C.b为正极,c为阴极,B是O2
D.E室最终得到Al(OH)3和CuO
【答案】A
【解析】
电解过程中C极室无色溶液变红,则发生反应2H2O+2e-==2OH-+H2↑,从而确定c电极为阴极,则d电极为阳极,发生反应2H2O-4e- ==O2↑+4H+。
A.D室发生反应:2H2O-4e-=4H++O2↑,Cr2O72-通过阴离子膜进入D室,发生反应Cr2O72-+H2O![]() 2CrO42-+2H+,所得含铬元素的微粒是Cr2O72-和CrO42-,A错误;
2CrO42-+2H+,所得含铬元素的微粒是Cr2O72-和CrO42-,A错误;
B.在C极室发生反应2H2O+2e- ==2OH-+H2↑,浆液中K+移向C室,C室产物是KOH和H2,B正确;
C.由以上分析可知,c为阴极,则a为负极,b为正极,B是O2,C正确;
D.E室K+移向阴极,Cr2O72-移向阳极,最终得到Al(OH)3和CuO,D正确;
故选A。

练习册系列答案
相关题目