题目内容
【题目】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途.回答下列问题: 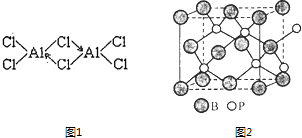
(1)写出基态镓原子的电子排布式 .
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图1缔合双分子Al2Cl6中Al原子的轨道杂化类型是 .
(3)B原子的电子有个不同的能级;晶体硼熔点为2300℃,则其为晶体.
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得.BP晶胞如图2所示. ①画出三溴化硼和三溴化磷的空间结构式.
三溴化硼三溴化磷
②在BP晶胞中B的堆积方式为 .
③计算当晶胞晶格参数为apm(即图中立方体的每条边长为apm)时,磷化硼中硼原子和磷原子之间的最近距离 .
【答案】
(1)1s22s22p63s23p63d104s24p1
(2)sp3
(3)3;原子
(4)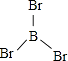 ;
; ![]() ;面心立方最密堆积;
;面心立方最密堆积; ![]() pm
pm
【解析】解:(1)Ga处于第四周期第ⅢA族,根据能量最低原理,其核外电子排布式为:1s22s22p63s23p63d104s24p1,
所以答案是:1s22s22p63s23p63d104s24p1;(2)由双分子Al2Cl6的结构可知,分子中Al原子形成4个σ键,没有孤对电子,杂化轨道数目为4,Al原子采取sp3杂化,
所以答案是:sp3;(3)B原子核外电子排布式为1s22s22p1,有3个不同的能级,晶体硼熔点为2300℃,熔点很高,属于原子晶体,
所以答案是:3;原子;(4)①BBr3中硼原子的价层电子对数为3+ ![]() =3,没有孤电子对,所以分子空间构型为平面三角形,结构式为
=3,没有孤电子对,所以分子空间构型为平面三角形,结构式为 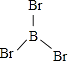 ;PBr3中磷原子的价层电子对数为3+
;PBr3中磷原子的价层电子对数为3+ ![]() =4,P原子有一对孤电子对,所以分子空间构型为三角锥形,结构式为:
=4,P原子有一对孤电子对,所以分子空间构型为三角锥形,结构式为: ![]() ,
,
所以答案是:  ;
; ![]() ;
;
②由晶胞结构可知,B原子处于晶胞顶点与面心,在BP晶胞中B的堆积方式为面心立方最密堆积,
所以答案是:面心立方最密堆积;
③P原子与周围的4个B原子最近且形成正四面体结构,二者连线处于体对角线上,为体对角线的 ![]() ,立方体的每条边长为a pm,则晶胞体对角线长为
,立方体的每条边长为a pm,则晶胞体对角线长为 ![]() a pm,则P原子与B原子最近距离为
a pm,则P原子与B原子最近距离为 ![]() a pm×
a pm× ![]() =
= ![]() pm,
pm,
所以答案是: ![]() pm.
pm.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】将不可再生的天然气、石油、煤等化石燃料转化利用、提高利用率已成为当务之急.
(1)根据部分键能数据和CH4 (g)+4F2 (g)=CF4(g)+4HF(g)的反应热△H为1940kJmol﹣1 , 计算H﹣F键的键能为 .
化学键 | C﹣H | C﹣F | H﹣F | F﹣F |
键能/(kJ.mol﹣1) | 414 | 489 | ? | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,二者均可利用CO和H2反应合成. ①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:CH3OCH3+6CO32﹣﹣12e﹣═8CO2+3H2O.写出该燃料电池的正极反应式 .
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2 . 某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式 .
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生H2S废气. ①电解池中电极A、B均为惰性电极,其中A为电解池的极;电极B所得到的物质X的分子式为 .
②反应池中发生的离子反应方程式为 . 
【题目】以黄铜矿(主要成分二硫化亚铁铜CuFeS2)为原料,用Fe2(SO4)3溶液作浸取剂提取铜,总反应的离子方程式是CuFeS2+4Fe3+Cu2++5Fe2++2S.
(1)该反应中,Fe3+体现性.
(2)上述总反应的原理如图1所示.负极的电极反应式是 .
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
实验 | 操作 | 2小时后Cu2+浸出率/% |
I | 加入足量0.10molL﹣1 Fe2(SO4)3溶液 | 78.2 |
II | 加入足量0.10molL﹣1 Fe2(SO4)3溶液,通入空气 | 90.8 |
III | 加入足量0.10molL﹣1 Fe2(SO4)3溶液,再加入少量0.0005molL﹣1 Ag2SO4溶液 | 98.0 |
①对比实验 I、II,通入空气,Cu2+浸出率提高的原因是 .
②由实验 III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+═Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+═2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005molL﹣1 Ag2SO4溶液,充分混合后静置.取上层清液,加入稀盐酸,观察到溶液中 , 证明发生反应 i.
b.取少量Ag2S粉末,加入溶液,充分混合后静置.取上层清液,加入稀盐酸,有白色沉淀,证明发生反应 ii.
(4)用实验 II的浸取液电解提取铜的原理如图2所示: 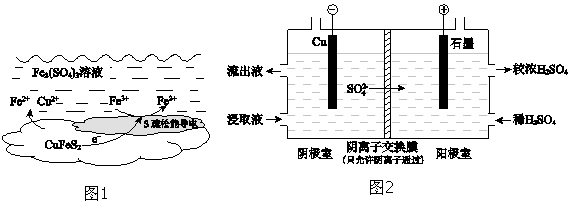
①电解初期,阴极没有铜析出.用电极反应式解释原因是 .
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是 .
【题目】下图是元素周期表的一部分,元素①~⑨在周期表中的位置如图所示(序号代表对应的元素)。
① | |||||||||||||||||
② | ③ | ④ | ⑤ | ||||||||||||||
⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
…… | |||||||||||||||||
(1)④在周期表中位于第_____周期_____族。
(2)9种元素中原子半径最大的是______(填元素符号),非金属性最强的是______(填元素符号);
(3)最高价氧化物对应水化物的碱性⑥_____⑦(填“>”或“<”)。
(4)⑧的阴离子的结构示意图为______;③的简单氢化物与⑧的最高价氧化物对应水化物化合生成的盐的化学式为_______。