题目内容
5.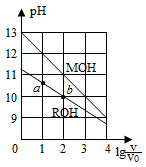 浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )| A. | MOH的碱性强于ROH的碱性 | |
| B. | ROH的电离程度:b点大于a点 | |
| C. | 若两溶液无限稀释,则它们的c(OH-)相等 | |
| D. | 当lg$\frac{V}{{V}_{0}}$=2时,若两溶液同时升高温度,则$\frac{c({M}^{+})}{c({R}^{+})}$增大 |
分析 A.相同浓度的一元碱,碱的pH越大其碱性越强;
B.弱电解质在水溶液中随着浓度的减小其电离程度增大;
C.若两种溶液无限稀释,最终其溶液中c(OH-)接近于纯水中c(OH-);
D.MOH的碱性强于ROH的碱性,当lg$\frac{V}{{V}_{0}}$=2时,若两溶液同时升高温度,促进弱电解质电离.
解答 解:A.相同浓度的一元碱,碱的pH越大其碱性越强,根据图知,未加水时,相同浓度条件下,MOH的pH大于ROH的pH,说明MOH的电离程度大于ROH,则MOH的碱性强于ROH的碱性,故A正确;
B.由图示可以看出ROH为弱碱,弱电解质在水溶液中随着浓度的减小其电离程度增大,b点溶液体积大于a点,所以b点浓度小于a点,则ROH电离程度:b>a,故B正确;
C.若两种溶液无限稀释,最终其溶液中c(OH-)接近于纯水中c(OH-),所以它们的c(OH-)相等,故C正确;
D.根据A知,碱性MOH>ROH,当lg$\frac{V}{{V}_{0}}$=2时,由于ROH是弱电解质,升高温度能促进ROH的电离,所以c(M+)/c(R+)减小,故D错误;
故选D.
点评 本题考查弱电解质在水溶液中电离平衡,为高频考点,明确弱电解质电离特点、弱电解质电离程度与溶液浓度关系等知识点是解本题关键,易错选项是C,注意:碱无论任何稀释都不能变为中性溶液或酸性溶液,接近中性时要考虑水的电离,为易错点.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
16.下列物质中,在一定条件下既能跟乙醇反应,又能跟乙酸反应的是( )
| A. | Cu | B. | CuO | C. | CaCO3 | D. | NaHCO3 |
20.甲醇既是重要的化工原料,又可作为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H1=-99kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3=+41kJ.mol-1
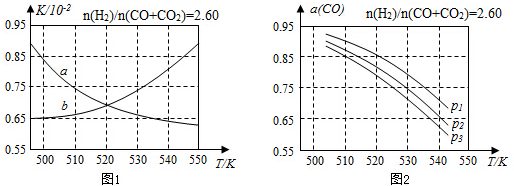
(2)反应①的化学平衡常数K的表达式为$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;图1中能正确反映平衡常数K随温度变化关系的曲线为a(填曲线标记字母),其判断理由是反应①正反应为放热反应,平衡常数随温度升高而减小.
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示.a(CO)值随温度升高而减小(填“增大”或“减小”),其原因是反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小.图2中的压强由大到小为P1>P2>P3,其判断理由是相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=-99kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3=+41kJ.mol-1
(2)反应①的化学平衡常数K的表达式为$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;图1中能正确反映平衡常数K随温度变化关系的曲线为a(填曲线标记字母),其判断理由是反应①正反应为放热反应,平衡常数随温度升高而减小.
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示.a(CO)值随温度升高而减小(填“增大”或“减小”),其原因是反应①正反应为放热反应,升高温度,平衡向逆反应方向移动,平衡体系中CO的量增大,反应③为吸热反应,升高温度,平衡向正反应方向移动,又使平衡体系中CO的增大,总结果,随温度升高,CO的转化率减小.图2中的压强由大到小为P1>P2>P3,其判断理由是相同温度下,反应③前后气体分子数不变,压强改变不影响其平衡移动,反应①正反应为气体分子数减小的反应,增大压强,有利于平衡向正反应方向移动,CO的转化率增大,故增大压强有利于CO的转化率升高

10.下列关于自然界中氮循环(如图)的说法不正确的是( )
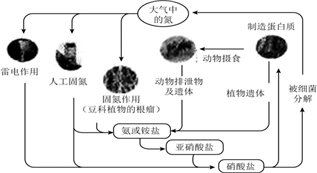

| A. | 氮元素均被氧化 | |
| B. | 工业合成氨属于人工固氮 | |
| C. | 含氮无机物和含氮有机物可相互转化 | |
| D. | 碳、氢、氧三种元素也参加了氮循环 |
12.常温下,对于pH=11的NaOH溶液,下列说法错误的是( )
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 该溶液中的c(OH-)=1.0×10-3mol•L-1 | |
| C. | 加水稀释104倍所得溶液显碱性 | |
| D. | 与pH=3的HF溶液等体积混合所得溶液:c(Na+)=c(F-)+c(HF) |
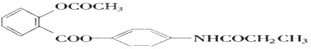 ,当它完全水解时,得到4种有机产物,它们的结构简式分别为
,当它完全水解时,得到4种有机产物,它们的结构简式分别为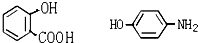 、CH3COOH、CH3CH2OH.
、CH3COOH、CH3CH2OH.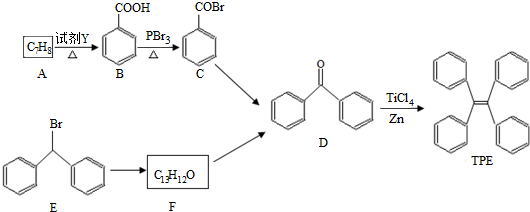
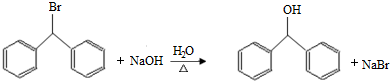 ;
;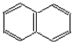 )的一元取代物;②存在羟甲基(-CH2OH),写出W所有可能的结构简式:
)的一元取代物;②存在羟甲基(-CH2OH),写出W所有可能的结构简式: ;
;



