题目内容
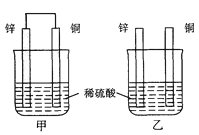
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
【答案】C
【解析】
试题分析:甲构成原电池,Zn易失电子作负极、Cu作正极,乙中不能构成闭合回路,所以不能构成原电池,则乙中Zn发生化学腐蚀,甲、乙中反应都是Zn+2H+=Zn2++H2↑,则A.甲中铜片是正极,铜片上氢离子放电生成氢气,乙中铜片不反应没有气体生成,A错误;B.乙中不能构成闭合回路,不能构成原电池,所以乙中Cu不是负极,B错误;C.甲、乙中反应都是Zn+2H+=Zn2++H2↑,所以两个烧杯中氢离子浓度都减小,则溶液的pH增大,C正确;D.构成原电池的反应速率大于发生化学腐蚀的反应速率,所以产生气泡的速度甲比乙快,D错误;答案选C。

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目