题目内容
下表是元素周期表的一部分,X、Y、Z、W均为短周期元素,
X、Z的质子数之和为21。下列说法正确的是
| | X | | Y |
| Z | | W | |
| A.X元素可形成六种氧化物 |
| B.Z元素在自然界中既有化合态,又有游离态 |
| C.X元素的氢化物的水溶液为酸性 |
| D.W元素的氧化物的水化物为强酸 |
A
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
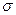 键和 个
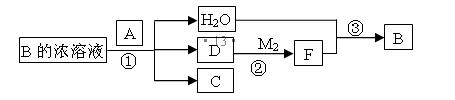
键和 个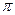 键。
键。 (3)a与b的元素形成的10电子中性分子X的空间构型为 ;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为 ,其中X与Ag+之间以 键结合。
(3)a与b的元素形成的10电子中性分子X的空间构型为 ;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为 ,其中X与Ag+之间以 键结合。
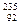 U只占0.724%。铀浓缩是指提高铀元素中
U只占0.724%。铀浓缩是指提高铀元素中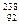 U化学性质的不同将二者分离
U化学性质的不同将二者分离 A中,X和Y元素的质量比为7:16,则A可以为 色的 (填化学式)。
A中,X和Y元素的质量比为7:16,则A可以为 色的 (填化学式)。