题目内容
对下列过程中发生反应的叙述正确的是
| A.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| B.Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质 |
| C.从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| D.从海水中提取溴单质的过程所涉及的反应均为置换反应 |
C
试题分析:A. 海水中的钾元素是钾离子,提取氯化钾固体,通过电解得到钾,发生了氧化还原反应,故A.错误; B.Na、Mg用电解熔融氯化物的方法来制备其单质。D海水提溴是先氧化溴离子为溴单质,再用还原剂(如SO2)还原溴单质为溴离子,再用氧化剂氧化溴离子为溴单质.此过程都是化学变化,但不均为置换反应。C铝土矿溶于NaOH溶液中发生Al2O3+2NaOH═2NaAlO2+H2O,没有元素的化合价变化,则不属于氧化还原反应,偏铝酸钠溶液的酸化发生AlO2-+H++H2O═Al(OH)3↓,没有元素的化合价变化,则不属于氧化还原反应,灼烧氢氧化铝固体发生2Al(OH)3
 Al2O3+3H2O,没有元素的化合价变化,也不属于氧化还原反应,C正确。
Al2O3+3H2O,没有元素的化合价变化,也不属于氧化还原反应,C正确。
练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
 2Hg+O2↑
2Hg+O2↑ 4Al+3O2↑
4Al+3O2↑ 2Cu+SO2
2Cu+SO2


 2Al+3Cl2↑
2Al+3Cl2↑ Mg+H2O
Mg+H2O Zn+CO2
Zn+CO2 
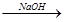 Mg(OH)2
Mg(OH)2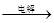 Mg
Mg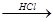 MgCl2溶液
MgCl2溶液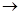 MgCl2熔融
MgCl2熔融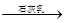 Mg(OH)2
Mg(OH)2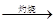 MgO
MgO