��Ŀ����
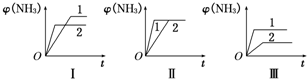
��֪ͨ���Ҵ���ȡ��������������·�ߣ�
a��CH3CH2OH(g)+H2O(g)==4H2(g)+2CO(g) ��H= +255.6kJ��mol��1
b��CH3CH2OH(g)+1/2O2(g)==3H2(g)+2CO(g) ��H= +13.8kJ��mol��1
������˵������ȷ����
A�������¶ȣ������b·�����Ҵ���ת����
B�����������ĵĽǶ�������b·�������������
C���Ҵ���ͨ�����۵�����ԭ�Ϸ����Ƶã����ڿ�������Դ
D����a��b֪��2H2(g)+O2(g)��2H2O(g)��H=��483.6kJ��mol��1
A
��������
���������Aѡ����¶ȣ��ή��b·�����Ҵ���ת���ʡ�Bѡ������b��Ӧ����ʱ��Ҫ���յ������٣����Դ��������ĵĽǶ�������b·���������������B��ȷ��C�Ҵ���ͨ�����۵�����ԭ�Ϸ����Ƶã����ڿ�������Դ��C��ȷ��Dѡ������ɸ�˹���������㣬Ҫ�õ�2H2(g)+O2(g)��2H2O(g)�����á�b��2a�����ԡ�H=��13.8kJ��mol��1��2��255.6kJ��mol��1= 483.6kJ��mol��1��D��ȷ��
���㣺��Դ����˹����
����������������Ȼ�ѧ����ʽ������������ת���ʣ���˹���ɵ����֪ʶ�������˸���֪ʶ����ۺϣ�����Ŀ�Ѷ�һ�㣬���ڼ��⡣

a��CH3CH2OH��g��+H2O��g���T4H2��g��+2CO��g����H=+255.6kJ?mol-1
b��CH3CH2OH��g��+
| 1 |
| 2 |
������˵������ȷ���ǣ�������
| A�������¶ȣ������b·�����Ҵ���ת���� |
| B�����������ĵĽǶ�������b·������������� |
| C���Ҵ���ͨ�����۵�����ԭ�Ϸ����Ƶã����ڿ�������Դ |
| D����a��b֪��2H2��g��+O2��g��=2H2O��g����H=-483.6kJ?mol-1 |