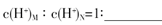题目内容
+2价金属元素M的原子中质子数比中子数少2个,2.1g的单质M与足量的盐酸反应共产生氢气0.05mol.试通过计算确定:
(1)该元素的摩尔质量为
(2)用 形式表示上题中金属元素M的原子
形式表示上题中金属元素M的原子
 .
.
(1)该元素的摩尔质量为
42g/mol
42g/mol
g/mol,(2)用
 形式表示上题中金属元素M的原子
形式表示上题中金属元素M的原子

分析:(1)根据电子守恒来计算元素的摩尔质量;
(2)元素符号左上角的数字为质量数,左下角的数字为质子数,质子数+中子数=质量数,以此来分析.
(2)元素符号左上角的数字为质量数,左下角的数字为质子数,质子数+中子数=质量数,以此来分析.
解答:解:(1)设+2价金属元素M的摩尔质量为x,
由2.1g的单质M与足量的盐酸反应共产生氢气0.05mol,
根据电子守恒可知,
×2=0.05mol×2×1,
解得x=42g/mol,故答案为:42g/mol;
(2)设该原子的质子数为y,由+2价金属元素M的原子中质子数比中子数少2个,
则y+(y+2)=42,
解得y=20,为钙元素,元素符号为Ca,
原子可表示为 ,故答案为:
,故答案为: .
.
由2.1g的单质M与足量的盐酸反应共产生氢气0.05mol,
根据电子守恒可知,
| 2.1g |
| x |
解得x=42g/mol,故答案为:42g/mol;
(2)设该原子的质子数为y,由+2价金属元素M的原子中质子数比中子数少2个,
则y+(y+2)=42,
解得y=20,为钙元素,元素符号为Ca,
原子可表示为
 ,故答案为:
,故答案为: .
.点评:本题考查学生利用金属与酸的反应进行计算,正确应用电子守恒可快速解答,省略书写化学反应方程式的麻烦,难度不大.

练习册系列答案
相关题目
图表法、图象法是常用的科学研究方法.
(Ⅰ)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量.从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推.
现有5种元素L、M、N、O、P,其I1~I3分别如下表,根据表中数据判断其中的金属元素有______,稀有气体元素是______,最活泼的金属是______,显二价的金属是______.
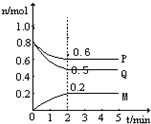
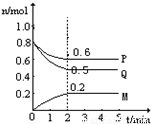
(Ⅱ)某温度时,在一个5L的密闭容器中,M、P、Q三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
(1)该反应的化学方程式为______
(2)若M、P、Q均为气体,反应达平衡时:
①体系的压强是开始时的______倍;从反应开始到平衡气体M的平均反应速率为______
②若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为______反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均分子量比原平衡时______(填增大、减小或相等).
(3)此反应达平衡后,若只加大体系压强,M的物质的量增加,若M是气体,则Q的聚集状态是______.
(Ⅰ)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量.从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推.
现有5种元素L、M、N、O、P,其I1~I3分别如下表,根据表中数据判断其中的金属元素有______,稀有气体元素是______,最活泼的金属是______,显二价的金属是______.
| 元 素 | I1/eV | I2/eV | I3/eV |
| L | 13.0 | 23.9 | 40.0 |
| M | 4.3 | 31.9 | 47.8 |
| N | 5.7 | 47.4 | 71.8 |
| O | 7.7 | 15.1 | 80.3 |
| P | 21.6 | 41.1 | 65.2 |
(1)该反应的化学方程式为______
(2)若M、P、Q均为气体,反应达平衡时:
①体系的压强是开始时的______倍;从反应开始到平衡气体M的平均反应速率为______
②若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为______反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均分子量比原平衡时______(填增大、减小或相等).
(3)此反应达平衡后,若只加大体系压强,M的物质的量增加,若M是气体,则Q的聚集状态是______.

 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题: