题目内容
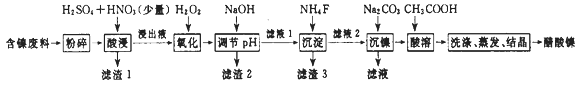
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
金属离子 | 开始沉淀时的pH | 沉淀完全时的pH | 物质 | 20℃时溶解性(H2O) | |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 | |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 | |
Al3+ | 3.0 | 5.0 | CaF2 | 难溶 | |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=1.0×10-5 |
(1)将含镍废料粉碎的目的是_______________________________________________。
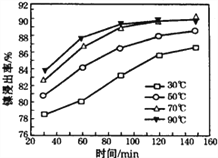
(2)“酸浸”实验中,镍的浸出率结果如图所示,从能量损耗和成本角度考虑,若要使镍的浸出效果最佳,选择的最好温度和时间分别为______℃、______ min。
(3)实验过程中,滤渣1主要成分的化学式为________、________。
(4)调节pH步骤中,溶液pH的调节范围是_____~______。选择此范围的目的是__________________________________。
(5)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:______________________________。
(6)沉镍过程中,若c(Ni2+)=4.0 mol·L-1,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],则需要加入Na2CO3固体的质量最少为_____g。(保留小数点后1位有效数字)
【答案】 增大固液接触面积,提高镍的浸出率 70 120 SiO2 CaSO4 5.0 6.7 使Al3+、Fe3+转化为沉淀,二不能使Ni2+转化为沉淀 NiS+H2SO4+2HNO3=NiSO4+SO2↑+2NO↑+2H2O 53.0
【解析】含镍废料(含 NiS、Al2O3、FeO、CaO、SiO2)粉碎,加硫酸和硝酸酸浸,过滤,滤渣1为二氧化硅和硫酸钙,浸出液含有Ni2+、Fe2+、Al3+、Ca2+,加H2O2把亚铁离子氧化为Fe3+,然后加NaOH调节pH,使Al3+、Fe3+转化为沉淀,同时Ni2+不能转化为沉淀,所以调节pH的范围5.0≤pH<6.7,过滤,滤渣2为氢氧化铁和氢氧化铝,滤液中含有Ni2+、Ca2+,再加氟化铵,生成CaF2沉淀,过滤,滤渣3为CaF2,滤液中加碳酸钠生成NiCO3沉淀,过滤,滤渣中加醋酸溶解,生成(CH3COO)2Ni溶液,然后蒸发浓缩、冷却结晶得到(CH3COO)2Ni固体;(1)将含镍废料粉碎的目的是增大固液接触面积,提高镍的浸出率;(2)由图象可知,为70℃、120min时,酸浸出率最高;(3)由流程分析可知,滤渣1为SiO2和CaSO4;(4)调节pH使Al3+、Fe3+转化为沉淀,同时Ni2+不能转化为沉淀,根据表中的数据可知,调节pH的范围为5.0≤pH<6.7;(5)酸浸过程中,1mol NiS被硝酸氧化失去6NA个电子,同时生成两种无色有毒气体,则生成NO和SO2,其反应的化学方程式为:NiS+H2SO4+2HNO3=NiSO4+SO2↑+2NO↑+2H2O;(5)已知NiCO3的Ksp=9.6×10-4,使100mL该滤液中的Ni2+沉淀物完全,即[c(Ni2+)≤10-5molL-1],则溶液中c(CO32-)=![]() =
=![]() mol/L=1mol/L,与Ni2+反应的n(CO32-)=cV=4.0mol/L×0.1L=0.4mol,则加入的碳酸钠的总物质的量n(CO32-)=0.4mol+1mol/L×0.1L=0.5mol,所以m=nM=0.5mol×106g/mol=5.3g。
mol/L=1mol/L,与Ni2+反应的n(CO32-)=cV=4.0mol/L×0.1L=0.4mol,则加入的碳酸钠的总物质的量n(CO32-)=0.4mol+1mol/L×0.1L=0.5mol,所以m=nM=0.5mol×106g/mol=5.3g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案

