题目内容
9.下列电离方程式正确的是( )| A. | H2O→H++0H- | B. | H2S→?2H++S2- | ||
| C. | CH3C00H?H++CH3C00- | D. | NaHC03→Na++H++C032- |
分析 A.水是弱电解质,电离方程式用可逆号;
B.氢硫酸为二元弱酸,电离方程式需要分步写;
C.醋酸在溶液中部分电离出醋酸根离子和氢离子;
D.碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开.
解答 解:A.水的电离为可逆反应,其正确的电离方程式为:H2O?H++0H-,故A错误;
B.氢硫酸在溶液中的电离分步进行,只要以第一步为主,其正确的电离方程式为:H2S?H++HS-,故B错误;
C.醋酸在溶液中存在电离平衡,其电离方程式为:CH3C00H?H++CH3C00-,故C正确;
D.碳酸氢钠为强电解质,在溶液中完全电离出钠离子和碳酸氢根离子,其正确的电离方程式为:NaHCO3=Na++HC03-,故D错误;
故选C.
点评 本题考查了电离方程式的书写,题目难度中等,明确强弱电解质的判断方法为解答关键,注意掌握电离方程式的书写原则,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
19.下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| C. | 2NO2=O2+2NO△H=+116.2kJ/mol(反应热) | |
| D. | S(s)+O2(g)═SO2(g)△H=-296.8kJ/mol(反应热) |
17.下列化学式能表示物质分子的是( )
| A. | KCl | B. | SiO2 | C. | HNO3 | D. | Fe |
4.如表是元素周期表的一部分,针对表中的①~⑩十种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:氩(填元素名称).元素⑨在周期表中的位置为第四周期第IA族.
(2)①②③三种元素形成的气态氢化物中,最稳定的是H2O(填化学式),④⑤⑨三种元素最高价氧化物的水化物中,碱性最强的是KOH(填化学式).
(3)③④⑤⑥四种元素形成的简单离子,离子半径由大到小的顺序是S2->O2->Na+>Al3+.(用离子符号表示)
(4)元素①和③形成的三原子化合物的结构式为:O=C=O,元素②的氢化物的电子式为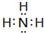 ,写出实验室制取该氢化物的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;△\;}}{\;}$CaCl2+2NH3↑+2H2O.
,写出实验室制取该氢化物的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;△\;}}{\;}$CaCl2+2NH3↑+2H2O.
(5)元素④与⑥形成的化合物属于离子(填“离子”、“分子”或“原子”)晶体,用电子式表示该化合物的形成过程: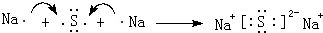 .
.
(6)用一个化学方程式说明⑥和⑦的非金属性相对强弱:Cl2+H2S=2HCl+S↓或Cl2+Na2S=2NaCl+S↓.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)①②③三种元素形成的气态氢化物中,最稳定的是H2O(填化学式),④⑤⑨三种元素最高价氧化物的水化物中,碱性最强的是KOH(填化学式).
(3)③④⑤⑥四种元素形成的简单离子,离子半径由大到小的顺序是S2->O2->Na+>Al3+.(用离子符号表示)
(4)元素①和③形成的三原子化合物的结构式为:O=C=O,元素②的氢化物的电子式为
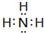 ,写出实验室制取该氢化物的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;△\;}}{\;}$CaCl2+2NH3↑+2H2O.
,写出实验室制取该氢化物的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;△\;}}{\;}$CaCl2+2NH3↑+2H2O.(5)元素④与⑥形成的化合物属于离子(填“离子”、“分子”或“原子”)晶体,用电子式表示该化合物的形成过程:
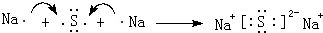 .
.(6)用一个化学方程式说明⑥和⑦的非金属性相对强弱:Cl2+H2S=2HCl+S↓或Cl2+Na2S=2NaCl+S↓.
14.氯水的pH( )
| A. | 小于7 | B. | 等于7 | C. | 大于7 |
15.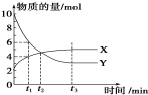 在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴、阳两极生成的气体的物质的量之比是1:1 | |
| C. | 总反应可表示为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2 | |
| D. | 阴极的反应式是:H2O+2e-═H2+O2ˉ CO2+2e-═CO+O2ˉ |
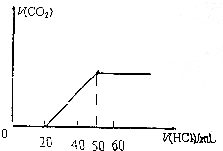 Ⅰ.取10mL密度1.20g/cm3、质量分数36.5%的y盐酸,加水稀释至300mL,则稀释后盐酸的物质的量浓度是0.4mol/L;
Ⅰ.取10mL密度1.20g/cm3、质量分数36.5%的y盐酸,加水稀释至300mL,则稀释后盐酸的物质的量浓度是0.4mol/L;