题目内容
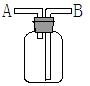
下列各组气体中,在通常情况下能共存且都能用浓硫酸干燥的是
| A.SO2、H2S | B.NO2、O2 |
| C.HCl、HBr | D.H2S、CO2 |
B
正确答案:B
A.SO2、H2S 不共存:SO2+2H2S=3S+2H2O B.正确; C. HCl、HBr 中HBr能被浓硫酸氧化成Br2;D.H2S、CO2中H2S能被浓硫酸氧化成S。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目


 G H I
G H I
 入气体形成微型气泡,将刚生成的四氧化三铁微粒包围,来阻止微粒的长大或聚集成团;② ▲ 。
入气体形成微型气泡,将刚生成的四氧化三铁微粒包围,来阻止微粒的长大或聚集成团;② ▲ 。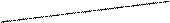
 滴定,至终点时消耗KMnO4溶液体积29.80mL。
滴定,至终点时消耗KMnO4溶液体积29.80mL。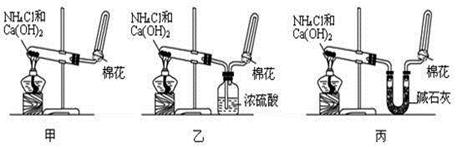
 )检验氨气是否收集满的方法是(简述操作方法、现象和结
)检验氨气是否收集满的方法是(简述操作方法、现象和结 论)____________________
论)____________________ 用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
 制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:将 ,
制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:将 , (填“大”或“小”),有 气味。
(填“大”或“小”),有 气味。