题目内容
【题目】Ⅰ.从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。

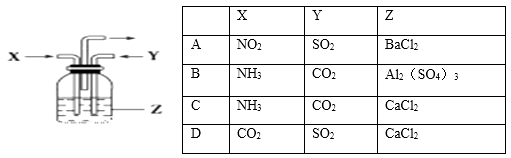
(1)海水中所得粗盐中含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,下列试剂加入的先后顺序正确的是_______
A. BaCl2→Na2CO3→NaOH→HCl B. NaOH→BaCl2→Na2CO3→HCl
C. Na2CO3→NaOH→BaCl2→HCl D. BaCl2→NaOH→Na2CO3→HCl
(2)为了检验精盐中是否含有SO42-,正确的方法是____________________________。
(3)写出电解饱和NaCl溶液的化学方程式____________________________________。
Ⅱ.海藻中提取碘的流程如图:
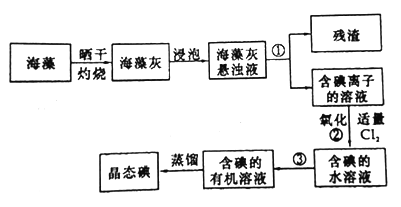
(4)指出提取碘的过程中有关实验操作名称:①__________,③___________;
(5)步骤②反应的离子方程式为_______________________________。
(6)下列关于海藻提取碘的说法,正确的是_____________
A.海藻的灼烧可以在蒸发皿中进行
B.含碘的有机溶液呈现出紫红色
C.操作③中先放出下层液体,然后再从下口放出上层液体
D.蒸馏操作时,温度计的水银球应伸入液面以下但不能触碰到蒸馏烧瓶的底部
【答案】 ABD 取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有SO42- 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 过滤 萃取分液 Cl2+2I-=2Cl-+I2 B
2NaOH+H2↑+Cl2↑ 过滤 萃取分液 Cl2+2I-=2Cl-+I2 B
【解析】(1)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后过滤后向滤液加入盐酸酸化。但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,答案选ABD;(2)检验精盐中是否含有SO42-的方法是取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有SO42-。(3)电解饱和NaCl溶液的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
Ⅱ.(4)悬浊液中的残渣需要过滤除去;碘易溶在有机溶剂中,则③是萃取分液;(5)步骤②是氯气氧化溴离子,反应的离子方程式为Cl2+2I-=2Cl-+I2。(6)A.海藻的灼烧应该在坩埚中进行,A错误;B.碘易溶在有机溶剂中,含碘的有机溶液呈现出紫红色,B正确;C.操作③中先放出下层液体,然后关闭活塞,再从上口倒出上层液体,C错误;D.蒸馏操作时,温度计的水银球应放在蒸馏烧瓶的支管出口处,D错误,答案选B。