题目内容
用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是( )
| A.电子通过盐桥从乙池流向甲池 |
| B.铜导线替换盐桥,原电池仍继续工作 |
| C.开始时,银片上发生的反应是:Ag-e-=Ag+ |
| D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同 |
D
解析

练习册系列答案
相关题目
X、Y、Z、M、N代表五种金属,有以下反应:
①Y与M用导线连接放入稀硫酸中,M上冒气泡;
②M、N为电极,与N的盐溶液组成原电池,电子从M极流出,经过外电路,流入N极;
③Z+2H2O(冷水)=Z(OH)2+H2↑;
④水溶液中,X+Y2+=X2++Y。
则这五种金属的活动性由强到弱的顺序为( )
| A.Z>X>Y>M>N | B.Z>Y>X>M>N |
| C.Z>X>Y>N>M | D.X>Y>M>N>Z |
针对下图装置的说法中,正确是
| A.溶液中pH值明显下降 |
| B.铁片为正极,镀锌铁片为负极 |
| C.阴极的电极反应式:Fe-2e→Fe2+ |
| D.电子由锌经溶液流向铁 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是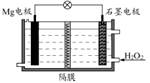
| A.Mg电极是该电池的正极 |
| B.石墨电极附近溶液的pH增大 |
| C.H2O2在石墨电极上发生氧化反应 |
| D.溶液中Cl-向正极移动 |
铜—锌—稀硫酸组成的原电池,放电一段时间后,溶液的pH将( )
| A.不变 | B.升高 |
| C.降低 | D.无法确定 |
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图。下列说法正确的是 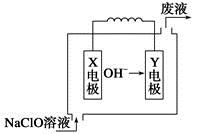
| A.镁作Y电极 |
| B.电池工作时,Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
D.X电极上发生的反应为ClO-+2H2O-4e-=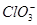 +4H+ +4H+ |
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有Fe2(SO4)3杂质的CuSO4溶液中加入适量的黑色粉末X,充分搅拌后过滤,将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )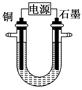
| A.黑色粉末X是铁粉 |
| B.铜电极连接电源正极 |
| C.石墨电极上发生的反应是4OH--4e-=O2↑+2H2O |
D.铜的相对原子质量的计算式是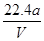 |
一种碳纳米管能够吸附氢气,可做二次电池(如下图所示)的碳电极。该电池的电解质为6 mol·L-1 KOH溶液,下列说法中正确的是 
| A.充电时阴极发生氧化反应 |
| B.充电时将碳电极与电源的正极相连 |
| C.放电时碳电极反应为H2-2e-=2H+ |
| D.放电时镍电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
| A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应 |
| B.负极的电极反应式为CH4+10OH--8e-=CO32—+7H2O |
| C.随着反应的进行,电解质溶液的pH保持不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的大 |