题目内容
| 物质 | 质量/g | 体积 | ||
| 0℃,101kPa | 20℃,101kPa | 0℃,202kPa | ||
| H2 | 2 | 22.4 | 24.0 | 11.2 |
| O2 | 32 | 22.4 | 24.0 | 11.2 |
| CO2 | 44 | 22.3 | 23.9 | 11.2 |
| A、物质的量相同的三种气体,在相同的条件下,其体积基本相同 |
| B、相同的条件下,体积相同的三种气体,其质量不同 |
| C、质量相同的三种气体,在相同的条件下,其体积一定不同 |
| D、相同的条件下,体积相同的三种气体,因其质量不同,所以气体分子数目也不同 |
B.相同的条件下,体积相同的三种气体,其物质的量相同,M不同,则其质量不同,故B正确;
C.质量相同的三种气体,由n=
| m |
| M |
D.相同的条件下,体积相同的三种气体,由n=
| V |
| Vm |
故选D.

 阅读快车系列答案
阅读快车系列答案Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3这三种分子的空间构型是 。
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子 。
(3)NaN3与KN3离子键强弱相比,NaN3 KN3(填“>”、“=”或“<” )。
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。
①写出氮化碳的化学式____ _ _____;
②指出氮化碳的晶体类型______ _____。
Ⅱ、分析表中四种物质的相关数据,请回答:
|
| CH4 | SiH4 | NH3 | PH3 |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
(1)CH4和SiH4比较,沸点高低的原因是____ _______;
(2)NH3和PH3比较,分解温度高低的原因是_____ ______;
(3)结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时___________先液化。
Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3这三种分子的空间构型是 。
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子 。
(3)NaN3与KN3离子键强弱相比,NaN3 KN3(填“>”、“=”或“<” )。
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。
①写出氮化碳的化学式____ _ _____;
②指出氮化碳的晶体类型______ _____。
Ⅱ、分析表中四种物质的相关数 据,请回答:
据,请回答:
| | CH4 | SiH4 | NH3 | PH3 |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
(2)NH3和PH3比较,分
 解温度高低的原因是_____ ______;
解温度高低的原因是_____ ______;(3)结合上述数据和规律判
 断,一定压强下HF和HCl的混合气体降温时___________先液化。
断,一定压强下HF和HCl的混合气体降温时___________先液化。 Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3这三种分子的空间构型是 。
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子 。
(3)NaN3与KN3离子键强弱相比,NaN3 KN3(填“>”、“=”或“<” )。
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。

①写出氮化碳的化学式____ _ _____;
②指出氮化碳的晶体类型______ _____。
Ⅱ、分析表中四种物质的相关数据,请回答:
|
|
CH4 |
SiH4 |
NH3 |
PH3 |
|
沸点/K |
101.7 |
161.2 |
239.7 |
185.4 |
|
分解温度/K |
873 |
773 |
1073 |
713.2 |
(1)CH4和SiH4比较,沸点高低的原因是____ _______;
(2)NH3和PH3比较,分解温度高低的原因是_____ ______ ;
(3)结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时___________先液化。
对于一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应的系列研究,请根据相关信息回答问题。
⑴关于反应物之间的定量关系的研究:
已知反应:Br2 +2Fe2+=2 Br -+2Fe3+,向10 mL0 .1mol/L的Fe Br2溶液中通入0 .003mol Cl2,该反应的离子方程式为
⑵关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg 2+)=
②科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。
一定温度下,在2L密闭容器中加入纳米级的Cu2O并通入0 .1mol水蒸气,发生反应:
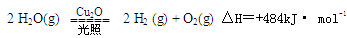 2 H2O(g)
2 H2O(g)
2 H2 (g) + O2(g) △H=+484kJ· mol-1,不同时段产生O2的量见下表:
|
时间/min |
20 |
40 |
60 |
80 |
|
n(O2)/mol |
0.0010 |
0.0016 |
0.0020 |
0.0020 |
则前20min的反应速率v(H2O)= ;达到平衡时,至少需要吸收的光能为 kJ。
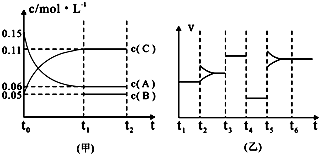
③向某密闭容器中加入0 .3molA、0 .1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示。附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件。已知t3~t4为使用催化剂,甲图中t0~t1阶段c (B)未画出。请回答:
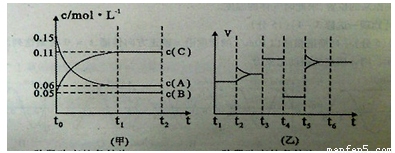
Ⅰ:t4~t5阶段改变的条件是 t5~t6阶段改变的条件是
Ⅱ:B的起始浓度为 ,该反应方程式为