题目内容
【题目】碳酸二甲酯[(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法不正确的是( )
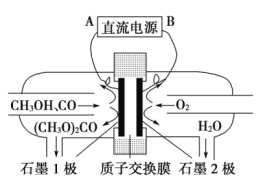
A.石墨2极与直流电源负极相连
B.石墨1极发生的电极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+
C.H+由石墨1极通过质子交换膜向石墨2极移动
D.电解一段时间后,阴极和阳极消耗的气体的物质的量之比为2:1
【答案】D
【解析】
该装置有外接电源,是电解池,由图可知,氧气在石墨2极被还原为水,则石墨2极为阴极,B为直流电源的负极,阴极反应式为O2+4H++4e-=2H2O,A为正极,石墨1极为阳极,甲醇和一氧化碳失电子发生氧化反应生成碳酸二甲酯,阳极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+,据此解答。
A. 由以上分析知,石墨2极为阴极,阴极与直流电源的负极相连,则B为直流电源的负极,故A正确;
B. 阳极上是甲醇和一氧化碳反应失电子发生氧化反应,电极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+,故B正确;
C. 电解池中,阳离子移向阴极,则H+由石墨1极通过质子交换膜向石墨2极移动,故C正确;
D. 常温常压下甲醇是液体,电解池工作时转移电子守恒,根据关系式2CO ~ 4e- ~ O2可知,阴极消耗的O2与阳极消耗的CO物质的量之比为1:2,故D错误;
答案选D。

练习册系列答案
相关题目