题目内容
已知黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去。该小组为测定黄钠铁矾的组成,进行了如下实验:
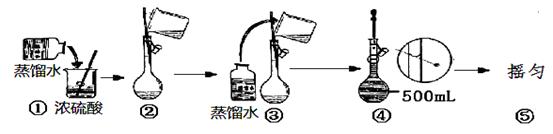
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)该小组不采用生成Fe(OH)3沉淀的方法除去铁元素,是因为生成的Fe(OH)3 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为 ,滴定到终点的颜色变化为 。
(3)通过计算确定黄钠铁矾的化学式(写出计算过程)。
①称取4.850 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
②量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
③另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165 g。
(1)该小组不采用生成Fe(OH)3沉淀的方法除去铁元素,是因为生成的Fe(OH)3 。
(2)用Na2S2O3溶液进行滴定时,使用的指示剂为 ,滴定到终点的颜色变化为 。
(3)通过计算确定黄钠铁矾的化学式(写出计算过程)。
(1)沉淀颗粒小、沉淀速率慢、不容易过滤等(合理答案均可)(2分)
(2)淀粉溶液(2分) 溶液蓝色恰好褪去,且半分钟内不再恢复(2分)
(3)NaFe3(SO4)2(OH)6(2分)
试题分析:(1)因为黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,所以不采用生成Fe(OH)3沉淀的方法除去铁元素,,是因为生成的Fe(OH)3不具备上述优点;(2)有碘单质参与的反应一般用淀粉溶液做指示剂,该滴定滴定碘溶液故现象为溶液蓝色恰好褪去,且半分钟内不再恢复;
(3)第(1)计算Fe3+的量n(Fe3+)=2n(I2) =n(Na2S2O3)="0.2500" mol·L-1×30.00 mL×10-3 L·mL-1=7.50×10-3 mol
第(2)计算SO42-的量n(SO42-)="1.165" g ÷233 g·mol-1=5.00×10-3 mol
根据电荷守恒和质量计算剩余离子的量
4.850-0.03×56-0.02×96=n(Na+)×23+n(OH-)×17
0.03×3+ n(Na+)=2×0.02+n(OH-)
n(Na+)="0.01" mol,n(OH-)="0.06" mol
计算各离子物质的量的关系x∶y∶m∶n=n(Na+)∶n(Fe3+)∶n(SO42-)∶n(OH-)=1∶3∶2∶6
得出化学式为NaFe3(SO4)2(OH)6。

练习册系列答案
相关题目
 2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1
2NH3(g)△H=-92.4 kJ·mol-1,当有3NA个电子转移时,△H变为-46.2 kJ·mol-1