题目内容
下列有关碳酸钠和碳酸氢纳的说法正确的是
- A.等质量的碳酸钠和碳酸氢钠分别与足量酸反应,前者产生的二氧化碳多
- B.足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生的二氧化碳一样多
- C.向饱和Na2CO3溶液中通入足量的CO2气体,有NaHCO3固体析出
- D.等质量的碳酸钠和碳酸氢钠,在水中电离出相同数目的Na+
C
分析:A、利用n= 计算碳酸钠和碳酸氢钠的物质的量,因酸足量,碳酸钠和碳酸氢钠完全反应,根据C原子守恒判断生成二氧化碳的量;
计算碳酸钠和碳酸氢钠的物质的量,因酸足量,碳酸钠和碳酸氢钠完全反应,根据C原子守恒判断生成二氧化碳的量;
B、等物质的量的盐酸,因盐足量,盐酸完全反应,利用2HCl~CO2,HCl~CO2来分析;
C、碳酸钠与CO2和水反应生成NaHCO3,NaHCO3溶解度小于Na2CO3;
D、利用n= 计算碳酸钠和碳酸氢钠的物质的量,再根据钠离子守恒判断.
计算碳酸钠和碳酸氢钠的物质的量,再根据钠离子守恒判断.
解答:A、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、 mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的
mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的
CO2的物质的量分别为1mol、 mol,故A错误;
mol,故A错误;
B、盐酸分别与足量碳酸钠和碳酸氢钠,因盐酸不足且相等,根据2HCl~CO2,HCl~CO2可知前者产生二氧化碳是后者的一半,故B错误;
C、碳酸钠与CO2和水反应生成酸式盐NaHCO3,NaHCO3溶解度小于Na2CO3,并且反应生成的NaHCO3固体质量比原来Na2CO3多,溶剂质量减少,溶液中有NaHCO3固体析出,故C正确;
D、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、 mol,根据钠离子守恒,二者电离出Na+的物质的量分别为2mol、
mol,根据钠离子守恒,二者电离出Na+的物质的量分别为2mol、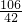 mol,故D错误.
mol,故D错误.
故选:C.
点评:本题考查Na2CO3和NaHCO3性质、难度中等,注意NaHCO3溶解度小于Na2CO3,Na2CO3与盐酸反应与量、顺序有关.
分析:A、利用n=
 计算碳酸钠和碳酸氢钠的物质的量,因酸足量,碳酸钠和碳酸氢钠完全反应,根据C原子守恒判断生成二氧化碳的量;
计算碳酸钠和碳酸氢钠的物质的量,因酸足量,碳酸钠和碳酸氢钠完全反应,根据C原子守恒判断生成二氧化碳的量;B、等物质的量的盐酸,因盐足量,盐酸完全反应,利用2HCl~CO2,HCl~CO2来分析;
C、碳酸钠与CO2和水反应生成NaHCO3,NaHCO3溶解度小于Na2CO3;
D、利用n=
 计算碳酸钠和碳酸氢钠的物质的量,再根据钠离子守恒判断.
计算碳酸钠和碳酸氢钠的物质的量,再根据钠离子守恒判断.解答:A、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、
 mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的
mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、
 mol,故A错误;
mol,故A错误;B、盐酸分别与足量碳酸钠和碳酸氢钠,因盐酸不足且相等,根据2HCl~CO2,HCl~CO2可知前者产生二氧化碳是后者的一半,故B错误;
C、碳酸钠与CO2和水反应生成酸式盐NaHCO3,NaHCO3溶解度小于Na2CO3,并且反应生成的NaHCO3固体质量比原来Na2CO3多,溶剂质量减少,溶液中有NaHCO3固体析出,故C正确;
D、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、
 mol,根据钠离子守恒,二者电离出Na+的物质的量分别为2mol、
mol,根据钠离子守恒,二者电离出Na+的物质的量分别为2mol、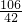 mol,故D错误.
mol,故D错误.故选:C.
点评:本题考查Na2CO3和NaHCO3性质、难度中等,注意NaHCO3溶解度小于Na2CO3,Na2CO3与盐酸反应与量、顺序有关.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
下列有关碳酸钠和碳酸氢钠的说法正确的是( )
| A、等质量的碳酸钠和碳酸氢钠分别与足量酸反应,前者产生的二氧化碳多 | B、足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生的二氧化碳一样多 | C、相同温度在水中的溶解度:碳酸钠>碳酸氢钠 | D、热稳定性:碳酸钠<碳酸氢钠 |
下列有关碳酸钠和碳酸氢钠的说法不正确的是( )
| A、热稳定性:碳酸钠>碳酸氢钠 | B、在水中的溶解度:碳酸钠<碳酸氢钠 | C、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 | D、足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生二氧化碳一样多 |
下列有关碳酸钠和碳酸氢纳的说法正确的是( )
| A、等质量的碳酸钠和碳酸氢钠分别与足量酸反应,前者产生的二氧化碳多 | B、足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生的二氧化碳一样多 | C、向饱和Na2CO3溶液中通入足量的CO2气体,有NaHCO3固体析出 | D、等质量的碳酸钠和碳酸氢钠,在水中电离出相同数目的Na+ |