题目内容
【题目】已知Ca3N2遇水发生水解反应,需密封保存。利用如下装置制取氮气,并用氮气制备Ca3N2,下列说法正确的是 ( )
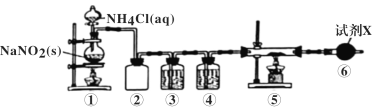
A.①中发生的反应属于置换反应
B.②的作用为安全瓶,防止停止加热时①中的溶液进入③中
C.③、④、⑥中依次盛装浓H2SO4、酸性氯化亚铁溶液、碱石灰
D.取⑤中少量产物,加适量蒸馏水,再滴加石蕊试液,溶液显蓝色
【答案】D
【解析】
由图可知,①中发生NaNO2+NH4Cl![]() NaCl+N2↑+2H2O,②可防止倒吸,作安全瓶,③中酸性FeCl2溶液可发生4Fe2++O2+4H+═4Fe3++2H2O,排除装置中氧气,防止与Ca反应,④中浓硫酸可干燥氮气,防止Ca与水反应,⑤中发生3Ca+N2
NaCl+N2↑+2H2O,②可防止倒吸,作安全瓶,③中酸性FeCl2溶液可发生4Fe2++O2+4H+═4Fe3++2H2O,排除装置中氧气,防止与Ca反应,④中浓硫酸可干燥氮气,防止Ca与水反应,⑤中发生3Ca+N2 Ca3N2,⑥中试剂X为碱石灰,可防止空气中水进入⑤中,以此来解答。
Ca3N2,⑥中试剂X为碱石灰,可防止空气中水进入⑤中,以此来解答。
A.根据分析可知①中发生的反应不属于置换反应,故A错误;
B.②的作用为安全瓶,可防止停止加热时③中液体进入①中,故B错误;
C.③、④、⑥中依次盛装酸性氯化亚铁溶液、浓H2SO4、碱石灰,先排除装置中氧气,防止与Ca反应,再干燥,故C错误;
D.实验结束后,取⑤中少量产物于试管中,加适量蒸馏水,发生反应Ca3N2+6H2O=2NH3↑+3Ca(OH)2↓,溶液显碱性,滴加石蕊试液,溶液变蓝,故D正确;
故选:D。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】高炉炼铁过程中发生反应: ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
A. 由表中数据可判断该反应:反应物的总能量<生成物的总能量
B. 1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO2表示该反应的平均速率为2×10-3/t mol·L-1·min-1
C. 为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D. 其他条件不变时,增加Fe2O3的用量,不能有效降低炼铁尾气中CO的含量