题目内容
下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
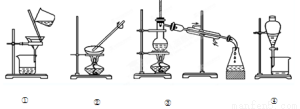
从海水中提取水:从KCl溶液中获取KCl晶体
分离CaCO3和水;分离植物油和水
练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
题目内容
下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)

从海水中提取水:从KCl溶液中获取KCl晶体
分离CaCO3和水;分离植物油和水
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案