题目内容
(2011?临沂模拟)图中B为日常生活中常见的金属,E是一种新型的清洁能源,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是生理盐水主要成分(图中部分反应物或生成物没有列出).
请按要求回答:
(1)写出B在周期表的位置第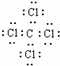
 .
.
(2)反应①的离子方程式为
(3)反应②进行的条件是
(4)反应③的化学方程式为

请按要求回答:
(1)写出B在周期表的位置第
三
三
周期ⅢA
ⅢA
族,G的电子式

(2)反应①的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(3)反应②进行的条件是
光照
光照
,过量Cl2
过量Cl2
.(4)反应③的化学方程式为
Al2O3+2NaOH═2NaAlO2+H2O
Al2O3+2NaOH═2NaAlO2+H2O
.分析:H、G是正四面体结构的非极性分子,H是一种重要的能源,则H为甲烷,由反应②可知G为CCl4,A为HCl;K是生理盐水主要成分,则K为NaCl,由反应④可知C为NaOH;B为金属,能与盐酸、与氢氧化钠反应,则B为Al,由框图中的转化可知E为氢气,D为氯化铝,F为偏铝酸钠,I为氢氧化铝,J为氧化铝;然后可依次解答各小问.
解答:解:H、G是正四面体结构的非极性分子,H是一种重要的能源,则H为甲烷,由反应②可知G为CCl4,A为HCl;K是生理盐水主要成分,则K为NaCl,由反应④可知C为NaOH;B为金属,能与盐酸、与氢氧化钠反应,则B为Al,由框图中的转化可知E为氢气,D为氯化铝,F为偏铝酸钠,I为氢氧化铝,J为氧化铝;
(1)因B为铝,位于周期表中第三周期第ⅢA族,G为CCl4,其电子式为 ,故答案为:三;ⅢA;
,故答案为:三;ⅢA; ;
;
(2)D为氯化铝,F为偏铝酸钠,则反应①的离子反应为Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)因烷烃的取代反应在光照条件下进行,为保证甲烷完全反应,则氯气应过量,故答案为:光照;过量Cl2;
(4)J为氧化铝,C为NaOH,则反应③的离子方程式为Al2O3+2NaOH═2NaAlO2+H2O,故答案为:Al2O3+2NaOH═2NaAlO2+H2O.
(1)因B为铝,位于周期表中第三周期第ⅢA族,G为CCl4,其电子式为
 ,故答案为:三;ⅢA;
,故答案为:三;ⅢA; ;
;(2)D为氯化铝,F为偏铝酸钠,则反应①的离子反应为Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)因烷烃的取代反应在光照条件下进行,为保证甲烷完全反应,则氯气应过量,故答案为:光照;过量Cl2;
(4)J为氧化铝,C为NaOH,则反应③的离子方程式为Al2O3+2NaOH═2NaAlO2+H2O,故答案为:Al2O3+2NaOH═2NaAlO2+H2O.
点评:本题考查无机物的推断,明确推断中转化的关系及物质的性质即可解答,明确推断突破口为H、K及B既能与酸反应又能与碱反应是解答本题的关键.

练习册系列答案
相关题目
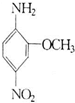 (2011?临沂模拟)2一氨基一5一硝基苯甲醚俗称红色基B,主要用于棉纤维织物的染色,也用于制金黄、枣红、黑等有机颜料,其结构简式如右所示.若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)可能为( )
(2011?临沂模拟)2一氨基一5一硝基苯甲醚俗称红色基B,主要用于棉纤维织物的染色,也用于制金黄、枣红、黑等有机颜料,其结构简式如右所示.若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)可能为( )