题目内容
2.用铂作电极电解AlCl3溶液的总反应离子方程式为2Al3++6Cl-+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑+3Cl2↑.分析 用Pt作电解电解AlCl3溶液时,阳极上氯离子放电生成氯气,阴极上水得电子生成氢气,同时阴极附近有OH-生成,OH-和Al3+反应生成生成沉淀Al(OH)3,据此书写离子方程式.
解答 解:用Pt作电解电解AlCl3溶液时,阳极上氯离子放电生成氯气,阴极上水得电子生成氢气,同时阴极附近有OH-生成,OH-和Al3+反应生成生成沉淀Al(OH)3,离子方程式为,
故答案为:2Al3++6Cl-+6H2O$\frac{\underline{\;电解\;}}{\;}$2Al(OH)3↓+3H2↑+3Cl2↑.
点评 本题以电解原理为载体考查离子方程式书写,为高频考点,明确离子放电顺序是解本题关键,OH-和Al3+反应生成沉淀为易错点,题目难度不大.

练习册系列答案
相关题目
13.向含有ag硝酸的稀溶液中,加入bg铁粉充分反应,铁粉全部溶解.已知有$\frac{a}{4}$g硝酸被还原,则a:b不可能是( )
| A. | 3:1 | B. | 9:2 | C. | 2:1 | D. | 4:1 |
10.下列说法正确的是( )
| A. | 如果5.6LN2含有n个氮分子,则NA一定约为4n | |
| B. | 18g水中所含的电子数是8NA | |
| C. | 在100mL0.5mol/L盐酸溶液中含有氯化氢分子数为0.05 NA | |
| D. | 23g Na+含有10mol电子 |
17.AgI沉淀中加过量K2S溶液,黄色色沉淀转化为黑色色沉淀,有关结论不正确的是( )
| A. | 加过量K2S溶液充分反应后,Ksp(AgI)减小 | |
| B. | 加过量K2S溶液充分反应后,溶液中Ag+ 和S2-的浓度之积等于Ksp(Ag2S) | |
| C. | 加过量K2S溶液充分反应后,溶液中Ag+ 和I- 的浓度之积小于Ksp(AgI) | |
| D. | Ksp(Ag2S)<Ksp(AgI) |
7.已知乙苯能在一定条件下发生下列过程,其中是因为苯环对侧链的影响而发生的是( )
| A. | 燃烧反应 | B. | 硝化反应 | ||
| C. | 与酸性高锰酸钾溶液作用 | D. | 加成反应 |
11.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 常温常压下,11.2L一氧化碳分子数是0.5NA | |
| B. | NA个氧气分子和NA个氮气分子的质量比为7:8 | |
| C. | 常温常压下,2.86gNa2CO3•10H2O含有的Na+数为0.02NA | |
| D. | 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,含有Cl-个数为NA |
16. 实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
有关数据见下表:
(1)A中加入沸石的作用是防止液体瀑沸.
(2)B中进水口为b(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下.
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?2HBr+H2SO4(浓)=Br2+SO2↑+2H2O(用化学方程式表示).
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是53.3%.
 实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色 液体 | 无色 液体 | 深红棕色 液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(2)B中进水口为b(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下.
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?2HBr+H2SO4(浓)=Br2+SO2↑+2H2O(用化学方程式表示).
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是53.3%.
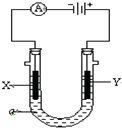 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: