题目内容
【题目】如图是浓硫酸与木炭的反应装置及验证其产物中含有SO2和CO2的装置.
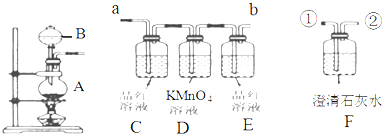
(1)仪器B的名称 ;
(2)写出浓硫酸与木炭在加热条件下反应的化学方程式 ;
(3)实验时,反应产生的气体应从端通入 (用“a”或“b”填空);反应产生的气体应从 端连接盛有澄清石灰水的实验装置(用“①”或“②”填空);
(4)C瓶的现象是 ;
(5)E瓶溶液的作用是 ;
(6)F瓶溶液发生的化学反应方程式为: ;
(7)完成D中的化学反应方程式:5SO2+2KMnO4+2═K2SO4+2MnSO4+2H2SO4,该反应的还原剂是 .
【答案】(1)分液漏斗(2)2H2SO4(浓)+C![]() 2SO2↑+CO2↑+2H2O(3)a;①(4)溶液褪色(5)检验SO2是否除尽(6)CO2+Ca(OH)2=CaCO3↓+H2O(7)SO2
2SO2↑+CO2↑+2H2O(3)a;①(4)溶液褪色(5)检验SO2是否除尽(6)CO2+Ca(OH)2=CaCO3↓+H2O(7)SO2
【解析】解:(1)由仪器图形可知B为分液漏斗,故答案为:分液漏斗;
(2)木炭粉与浓硫酸发生反应产生SO2和CO2气体,反应的方程式为2H2SO4(浓)+C![]() 2SO2↑+CO2↑+2H2O,
2SO2↑+CO2↑+2H2O,
故答案为:2H2SO4(浓)+C![]() 2SO2↑+CO2↑+2H2O;
2SO2↑+CO2↑+2H2O;
(3)实验时应从长导管进气,即从a端进,检验二氧化碳,应从①进入,故答案为:a;①;
(4)SO2具有漂白性,可使品红褪色,
故答案为:溶液褪色;
(5)要检验二氧化碳气体,应先除去SO2,并检验SO2是否除尽,实验流程中C用来检验SO2验气体,D除去SO2,E验证SO2是否除尽,F检验CO2;
故答案为:检验SO2是否除尽;
(6)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,方程式为CO2+Ca(OH)2=CaCO3↓+H2O,故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;
(7)反应中二氧化硫被氧化生成硫酸,二氧化硫为还原剂,故答案为:SO2.

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】有一包黑色粉末,可能由C、CuO、Fe三种物质中的一种或几种组成。某化学兴趣小组为了探究它的成分,按如下步骤进行实验。
(1)先对实验做了如下设想和分析:黑粉中只有碳粉不溶解于稀盐酸。取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况)。请你完成下表。
烧杯中可能出现的现象 | 结论 |
① | 只含C |
②固体部分溶解,溶液变成蓝色,无气泡 | |
③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含C、Fe |
(2)通过实验及分析,确定该粉末为C、CuO的混合物。为了进一步探究C、CuO的性质,他们又利用这种混合物补充做了下面两个实验。
【实验一】将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。烧杯中 (填“有”或“无”)不溶物,溶液呈 色。
【实验二】将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请回答:①烧杯中 (填“有”或“无”)不溶物;②若静置后溶液呈无色,则该溶液中溶质是 (写化学式);③若静置后溶液呈蓝色,该实验过程中所发生反应的化学方程式 、 。