题目内容
【题目】“结晶玫瑰”具有强烈的玫瑰香气,属于结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。“结晶玫瑰”的化学名称为乙酸三氯甲基苯甲酯,通常用三氯甲基苯基甲醇和醋酸酐为原料制备。

已知:
物质 | 在乙醇中的溶解性 | 在水中的溶解性 | 熔点℃ |
三氯甲基苯基甲醇 | 溶 | 不溶 | — |
醋酸酐 | 溶 | 溶 | -73 |
结晶玫瑰 | 溶 | 不溶 | 88 |
醋酸 | 易溶 | 易溶 | 16.6 |
部分实验装置以及操作步骤如下:

请根据以上信息,回答下列问题:
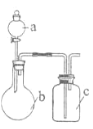
(1)装置中仪器B的名称是___________。
(2)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌。待混合均匀后,最适宜的加热方式为油浴加热,用油浴加热的理由是_______________。有同学认为装置中A仪器也可改为另一种漏斗,该漏斗的名称是___________,它的作用是____________。
现有同学设计如下方案把粗产品进行提纯。
(3)①将粗产品溶解在________(填“水”、“乙醇”或“粗产品滤液”)中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解,得到无色溶液。然后将所得溶液经过__________(填操作方法)析出白色晶体,整个过程中不需要用到的仪器是_______(选择相应字母填空)。
A.冷凝管 B.烧杯 C.蒸发皿 D.玻璃棒
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,请列举一种常见的实验室干燥的方法_______。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,实验现象为__________。
(4)ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰bg,则产率是_________。(用含a、b的式子表示)
【答案】三颈烧瓶 控制反应温度为110℃(大于100℃),且能使反应物均匀受热 恒压分液漏斗或恒压滴液漏斗 平衡气压,使液体顺利流下 乙醇 冷却结晶 C 空气中风干,空气中晾干,高温烘干,用滤纸吸干等 白色晶体在88℃左右完全熔化 ![]()
【解析】
三氯甲基苯基甲醇和醋酸酐放入三颈烧瓶,加入浓硫酸作催化剂,发生取代反应,为便于控制温度在110℃左右,需使用油浴加热;加热3小时后,反应基本完成,此时将反应混合液冷却,然后倒入冰水中,醋酸酐和醋酸溶解,而乙酸三氯甲基苯甲酯和少量三氯甲基苯基甲醇结晶析出;过滤后,得到粗产品。将粗产品溶于乙醇中均匀混合,用水浴加热到70℃,
再冷却结晶,过滤、洗涤、干燥,便可获得乙酸三氯甲基苯甲酯晶体。
(1)装置中,仪器B是具有三个颈的烧瓶,其名称是三颈烧瓶。答案为:三颈烧瓶;
(2)因为需加热温度为110℃,超出了水的沸点,所以最适宜的加热方式为油浴加热,用油浴加热的理由是控制反应温度为110℃(大于100℃),且能使反应物均匀受热。A仪器也可改为另一种漏斗,该漏斗应具有使液体容易滴下的作用,其名称是恒压分液漏斗或恒压滴液漏斗,它的作用是平衡气压,使液体顺利流下。答案为:控制反应温度为110℃(大于100℃),且能使反应物均匀受热;恒压分液漏斗或恒压滴液漏斗;平衡气压,使液体顺利流下;
(3)①因为粗产品中的成分难溶于水而易溶于乙醇,所以将粗产品溶解在乙醇中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解得到无色溶液,然后将所得溶液经过冷却结晶析出白色晶体。溶解时应使用烧杯、玻璃棒,水浴加热、回流溶剂时需使用冷凝管,所以整个过程中不需要用到的仪器是蒸发皿,故选C。
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,实验室干燥的方法可以是空气中风干、空气中晾干、高温烘干、用滤纸吸干等。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,因为结晶玫瑰是纯净物,所以温度在熔点附近时,晶体完全熔化,所以实验现象为白色晶体在88℃左右完全熔化。答案为:乙醇;冷却结晶;C;空气中风干,空气中晾干,高温烘干,用滤纸吸干等;白色晶体在88℃左右完全熔化;
(4)由反应方程式: ,理论上,ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰的质量为
,理论上,ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰的质量为![]() =
=![]() g,则产率是
g,则产率是 =
= ![]() 。答案为:
。答案为:![]() 。
。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】利用如图实验装置进行相关实验,能得出相应实验结论的是( )
a | b | c | 实验结论 |
| |
A | 浓醋酸 | CaCO3 | C6H5ONa溶液 | 酸性:碳酸>苯酚 | |
B | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯和液溴发生取代反应 | |
C | 浓盐酸 | 酸性KMnO4溶液 | 碘化钾溶液 | 氧化性:Cl2>I2 | |
D | 饱和食盐水 | 电石 | 酸性KMnO4溶液 | 乙炔具有还原性 |
A.AB.BC.CD.D