题目内容
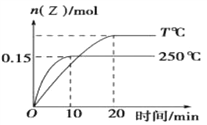
【题目】将 1mol X 和 2mol Y 充入容积为 1L 的密闭容器中,分别在 250℃和 T℃下发生反应:X(g)+2Y(g)![]() Z(g) △ H,Z 的物质的量随时间变化如右图。下列说法正确的是( )
Z(g) △ H,Z 的物质的量随时间变化如右图。下列说法正确的是( )
A. △ H > 0
B. 250 ℃时,0~l0min, v(Y)=0.015mol/(L·min)
C. 其他条件不变若减小容器体积,X 的体积分数增大
D. T℃,20min 时再充入 1molX 和 2molY,重新达到平衡时 Y 的转化率增大
【答案】D
【解析】A. 温度高反应速率快,达到平衡的时间短。根据图像可知250℃是首先达到平衡状态,则250℃>T℃,温度高Z的平衡量减少,说明升高温度平衡向逆反应方向进行,所以正反应放热,则△H<0,A错误;B. 250℃时,0~l0min内生成Z是0.15mol,根据方程式可知消耗Y是0.3mol,浓度是0.3mol/L,所以 v(Y)=0.3mol/L÷10min=0.03mol/(L·min),B错误;C. 其他条件不变,若减小容器体积,压强增大,平衡向正反应方向进行,X的体积分数减小,C错误;D. T℃,20min时再充入1molX和2molY相当于增大压强,平衡向正反应方向进行,重新达到平衡时Y的转化率增大,D正确,答案选D。

练习册系列答案
相关题目
【题目】下表中金属的冶炼原理与方法不完全正确的是( )
选项 | 冶炼原理 | 方法 |
A | 2HgO=2Hg+O2 | 热分解法 |
B | 2Al2O3 (熔融)=4Al+3O2 | 电解法 |
C | Cu2S+O2=2Cu+SO2 | 热分解法 |
D | Fe2O3 +2Al=2Fe+Al2O3 | 热还原法 |
A. AB. BC. CD. D