题目内容
【题目】下列各组物质中,将前者和后者混合时,无论前者是否过量,都能用同一个化学方程式表示的是( )
A.![]() 溶液,NaOH溶液B.稀
溶液,NaOH溶液B.稀![]() ,
,![]() 溶液
溶液
C.澄清石灰水,![]() D.氨水,
D.氨水,![]() 溶液
溶液
【答案】D
【解析】
A. ![]() 溶液、NaOH溶液混合,若前者少量,发生反应为Al3++4OH-=AlO2-+2H2O;若前者过量,发生反应为Al3++3OH-= Al(OH)3↓,不合题意。
溶液、NaOH溶液混合,若前者少量,发生反应为Al3++4OH-=AlO2-+2H2O;若前者过量,发生反应为Al3++3OH-= Al(OH)3↓,不合题意。
B. 稀![]() 、
、![]() 溶液混合,若前者过量,发生反应为AlO2-+4H+=Al3++2H2O;若后者过量,发生反应为AlO2-+H++H2O= Al(OH)3↓,不合题意。
溶液混合,若前者过量,发生反应为AlO2-+4H+=Al3++2H2O;若后者过量,发生反应为AlO2-+H++H2O= Al(OH)3↓,不合题意。
C. 澄清石灰水、![]() ,若前者过量,发生反应Ca(OH)2+CO2=CaCO3↓+H2O;若后者过量,发生反应Ca(OH)2+2CO2=Ca(HCO3)2,不合题意。
,若前者过量,发生反应Ca(OH)2+CO2=CaCO3↓+H2O;若后者过量,发生反应Ca(OH)2+2CO2=Ca(HCO3)2,不合题意。
D. 氨水、![]() 溶液,不管前者是否过量,发生的反应都是Al3++3NH3·H2O = Al(OH)3↓+3NH4+,因为氢氧化铝不溶于过量的氨水,符合题意。
溶液,不管前者是否过量,发生的反应都是Al3++3NH3·H2O = Al(OH)3↓+3NH4+,因为氢氧化铝不溶于过量的氨水,符合题意。
故答案为D。

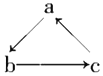
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是 ( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuSO4 | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A. AB. BC. CD. D
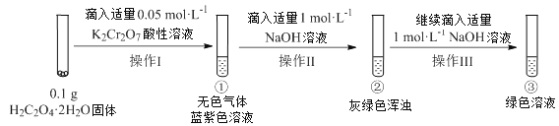
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) ![]() 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
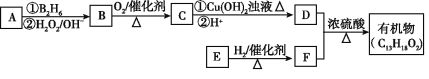
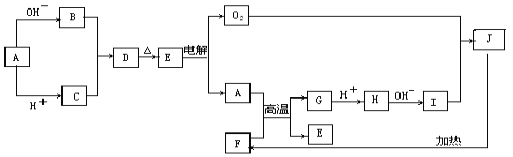
【题目】PdCl2广泛用作催化剂和一些物质的检测试剂。由Pd(NH3)2Cl2制备PdCl2工艺流程如图所示。

(1)肼(N2H4)可以被看作二元弱碱,结合质子生成N2H5+或N2H62+。肼与少量稀硫酸混合后,得到产物的化学式为___。
(2)对工艺流程图中的滤液处理办法最好的是:___
a.返到提钯废液中,循环使用 b.转化为无毒物质后排放 c.深埋于地下
(3)王水溶钯时,Pd被氧化为H2PdCl4。同时得到唯一还原产物亚硝酰氯(NOCl)。反应消耗的HCl与HNO3的物质的量之比为___。
(4)赶硝,是将残余的NO3浓度降低到不大于0.04%。实验数据记录如表:
表一:不同HCl用量和MxOy用量(每10gPd)与NO3残留量
HCl用量(mL) | MxOy用量(mL) | NO3含量(%) |
5 | 0、10、20、30、40 | 0.15、0.10、0.05、0.04、0.03 |
10 | 0、5、10、15、20 | 0.10、0.08、0.05、0.03、0.02 |
15 | 0、5、10、15、20 | 0.08、0.06、0.05、0.03、0.02 |
处理1吨Pd,需要用到HCl和MxOy的总体积至少为___m3(合理选择表格里相关数据计算)。
(5)煅烧过程发生分解反应,化学方程式为:___。
(6)浸有磷钼酸铵溶液的氯化钯试纸遇微量CO立即变成蓝色。原理较为复杂,第一步是CO还原PdCl2得到Pd单质,同时有常见的氧化物生成。写出反应原理中第一步的化学方程式:___