题目内容
8.下列各组物质的反应可用同一化学方程式或离子方程式表示的是( )| A. | 少量H2S通入NaOH溶液中;足量H2S通入NaOH溶液中 | |
| B. | 少量铁粉与硫粉共热;足量铁粉与硫粉共热 | |
| C. | 常温下Na与O2反应;Na在O2中点燃 | |
| D. | 铜与稀硝酸反应;铜与浓硝酸反应 |
分析 A.硫化氢与氢氧化钠溶液反应,产物与硫化氢用量有关;
B.铁粉与硫反应生成硫化亚铁;
C.钠与氧气反应产物与条件有关;
D.产物与硝酸浓度有关.
解答 解:A.硫化氢少量反应生成硫化钠和水,过量生成硫氢化钠,不能用同一个方程式表示,故A不选;
B.铁粉与硫反应生成硫化亚铁,与反应物用量无关,可以用同一个式子表示,故B选;
C.常温下反应生成氧化钠,燃烧生成过氧化钠,不能用同一个方程式表示,故C不选;
D.稀硝酸反应生成一氧化氮,浓硝酸反应生成二氧化氮,不能用同一个方程式表示,故D不选;
故选:B.
点评 本题考查离子反应方程式书写的正误判断,为高考经典题型,把握发生的反应及离子反应的书写方法为解答的关键,侧重反应物用量、反应条件等对反应的影响,题目难度不大

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
19.下列微粒的半径比值大于1的是( )
| A. | Mg2+/Mg | B. | K+/S2- | C. | N/P | D. | Cl-/Cl |
16.可逆反应A(g)+3B(g)═2C(g)+2D(g),在四种不同条件下的反应速率如下,其中反应速率最快的是( )
| A. | VA=0.15mol/(L•min) | B. | VB=0.6mol/(L•min) | ||
| C. | VC=0.4mol/(L•min) | D. | VD=0.6mol/(L•min) |
3.下列叙述正确的是( )
| A. | P4和NO2都是共价化合物 | |
| B. | 次氯酸的结构式为H-Cl-O | |
| C. | 在CaO和SiO2晶体中,都不存在单个小分子 | |
| D. | CCl4和NH4Cl都是以共价键结合的分子 |
13.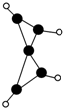 科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
 科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )| A. | X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色 | |
| B. | X是一种常温下能稳定存在的液态烃 | |
| C. | X和乙烷类似,都容易发生取代反应 | |
| D. | 充分燃烧等质量的X和甲烷,甲烷消耗氧气较多 |
20.鉴别食盐水和蔗糖水的方法:
(1)向两种溶液中加入少量稀硫酸并加热,再加氢氧化钠溶液中和硫酸,最后加入银氨溶液微热;
(2)测溶液导电性;
(3)将溶液与溴水混合,振荡;
(4)用舌头尝味道.
其中在实验室进行鉴别的正确方法是( )
(1)向两种溶液中加入少量稀硫酸并加热,再加氢氧化钠溶液中和硫酸,最后加入银氨溶液微热;
(2)测溶液导电性;
(3)将溶液与溴水混合,振荡;
(4)用舌头尝味道.
其中在实验室进行鉴别的正确方法是( )
| A. | (1)(2) | B. | (1)(3) | C. | (2)(3) | D. | (1)(2)(3)(4) |
17.下列有关实验的说法中错误的是( )
| A. | 在蒸馏的实验中,温度计的水银球位于支管口处是为了测出馏分的沸点 | |
| B. | 用直接蒸馏的方法可以得到无水乙醇 | |
| C. | 在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失 | |
| D. | 作为重结晶实验的溶剂,杂质在此溶剂中的溶解度受温度影响应该很大 |
18.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积缩小到原体积的一半,达到新的平衡后,B的浓度是原来的1.8倍,则( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率减小 | ||
| C. | 物质B的质量分数增加 | D. | a>b |